
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2 |
D
解析试题分析:由“W是短周期主族元素中原子半径最大的”结合同周期同主族原子半径递变规律知W为钠元素;X原子最外层电子数是核外电子层数的3倍,X为氧元素;又X、Z同族,Z为硫元素;Y的最高正价与最低负价代数和为6,知Y为第ⅦA元素,Y、Z同周期知Y为氯元素。即:X为氧元素、Y为氯元素、Z为硫元素、W为钠元素。A、Y(Cl)元素最高价氧化物对应的水化物化学式应为HYO4(HClO4),错误;B、原子半径由大到小的顺序应为为:W> Z>Y(Na>S>Cl),错误;C、氢化物的稳定性:HCl>H2S;错误;D、X与W形成的两种化合物为Na2O、Na2O2,阴、阳离子物质的量之比均为1︰2,正确。
考点:考查元素推断,“位---构---性”三者之间的关系


科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.Si是一种非金属主族元素,其晶体可用于制作计算机芯片 |
| B.工业上由NH3制碳铵属于氮的固定中的人工固氮 |
| C.Cl、Br、I的非金属性逐渐减弱,HCl、HBr、HI水溶液的酸性逐渐减弱 |
| D.S、P、Cl得电子能力和它们相应的最高价氧化物对应水化物的酸性均依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于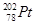 的说法正确的是
的说法正确的是
A.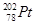 和 和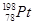 的质子数相同,互称为同位素 的质子数相同,互称为同位素 |
B.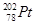 和 和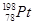 的中子数相同,互称为同位素 的中子数相同,互称为同位素 |
C.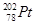 和 和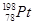 的核外电子数相同,是同一种核素 的核外电子数相同,是同一种核素 |
D.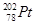 和 和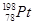 的质量数不同,不能互称为同位素 的质量数不同,不能互称为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
随着卤素原子半径的增加,下列递变规律正确的是( )
| A.单质的熔沸点逐渐降低 | B.卤素离子的还原性逐渐增强 |
| C.最高正化合价逐渐增大 | D.单质的氧化性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
1911年前后,英国物理学家卢瑟福用带正电的 粒子轰击极簿的金箔。为了解释实验结果,提出了原子的核式结构学说。下列图中,黑点表示金原子核的位置,曲线ab、cd和ef表示经过金原子核附近的
粒子轰击极簿的金箔。为了解释实验结果,提出了原子的核式结构学说。下列图中,黑点表示金原子核的位置,曲线ab、cd和ef表示经过金原子核附近的 粒子的运动轨迹,能正确反映实验结果的图是( )
粒子的运动轨迹,能正确反映实验结果的图是( )
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素M、X、Y、Z,其中X、Y、Z在周期表中所处的位置如图所示。M元素原子的最外层电子数为其次外层电子数的2倍。X、Y、Z三种元素原子质子数之和为32。则下列说法正确的是( )
| X | | Z |
| | Y | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
据报道,用10B合成的10B20有较好的抗癌作用。下列叙述正确的是
| A.10B20是一种新型化合物 | B.10B的中子数和核外电子数相等 |
| C.10B20晶体熔点高,硬度大 | D.10B和10B20互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、 Z、W在元素周期表中的位置如下表,且Z族元素的化合物种类最多。则下列说法正确的是
| | X | | Y |
| Z | | W | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com