
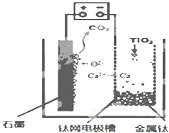
 �о����֣�������ʯī������������������������CaF2-CaO������ʣ�������ͼ��ʾװ�û�ý����ƣ����Ը�Ϊ��ԭ������ԭ���������Ʊ������ѣ�����������ȷ���ǣ�������
�о����֣�������ʯī������������������������CaF2-CaO������ʣ�������ͼ��ʾװ�û�ý����ƣ����Ը�Ϊ��ԭ������ԭ���������Ʊ������ѣ�����������ȷ���ǣ�������| A�� | ��TiO2�Ƶ�1mol ����Ti�����������·ת��2NA���� | |
| B�� | �����ĵ缫��ӦʽΪ��C+2O2--4e-�TCO2�� | |
| C�� | ����Ǧ��������װ�õĹ����Դ����+��������Ӧ����Pb�缫 | |
| D�� | ���Ʊ�������ǰ������װ����CaO���������� |
���� ����ͼ֪�������ϵ缫��ӦʽΪC+2O2--4e-�TCO2���������ϵ缫��ӦʽΪ��2Ca2++4e-�T2Ca���ƻ�ԭ�������ѷ�Ӧ����ʽΪ��2Ca+TiO2 $\frac{\underline{\;һ��������\;}}{\;}$Ti+2CaO����+��������Ӧ����ԭ���������
��� �⣺A����TiO2�Ƶ�1mol����Ti��TiԪ�ػ��ϼ���+4�۽��͵�0�ۣ������������·ת��4mol���ӣ���A����
B�������ϵ缫��ӦʽΪC+2O2--4e-�TCO2������B��ȷ��
C����+����ʾԭ������������ԡ�+��������Ӧ����ԭ�����������PbO2������C����
D�������ϵ缫��ӦʽΪ��2Ca2++4e-�T2Ca���ƻ�ԭ�������ѷ�Ӧ����ʽΪ��2Ca+TiO2=Ti+2CaO�����Ʊ�������ǰ������װ����CaO���������䣬��D����
��ѡB��
���� �����ۺϿ�����غ�ԭ���֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬ע����յ缫����ʽ����д��Ϊ��������Ŀ�Ĺؼ����Ѷ��еȣ�


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
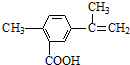
| A�� | ��һ�������£��ܷ���ȡ���������������ͼӾ۷�Ӧ | |
| B�� | �����ʷ�������������9��̼ԭ����ͬһƽ���� | |
| C�� | 1 mol������������4 mol H2�����ӳɷ�Ӧ | |
| D�� | 1 mol��������ȫ������������13 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
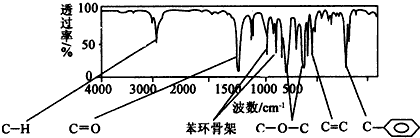
 ��
��
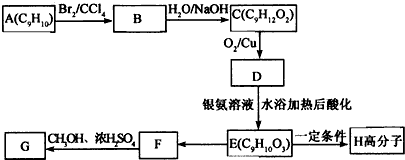
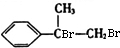 +2NaOH$��_{��}^{ˮ}$
+2NaOH$��_{��}^{ˮ}$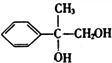 +2NaBr
+2NaBr
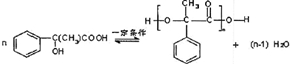
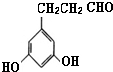
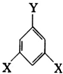 ��ʾ������X��Y����ΪH������д����������ͨʽ���ܷ���������Ӧ���������ʵĽṹ��ʽ��
��ʾ������X��Y����ΪH������д����������ͨʽ���ܷ���������Ӧ���������ʵĽṹ��ʽ��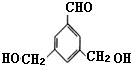 ��
�� ��
��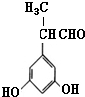 ��
��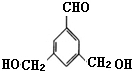 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10mL0.1 mol•L-1��AlCl3��Һ | B�� | 20mL0.1 mol•L-1��CaCl2��Һ | ||
| C�� | 30mL0.2 mol•L-1��KCl��Һ | D�� | 100mL0.25 mol•L-1��NaCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
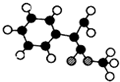
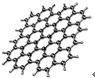 ��ʯī�з��������ʯīϩ����֪������Ӳ�����ʣ����Ƴɵ�������С�����ײ��ϣ���ṹ��ͼ��ʾ�����й���ʯīϩ��˵����ȷ���ǣ�������
��ʯī�з��������ʯīϩ����֪������Ӳ�����ʣ����Ƴɵ�������С�����ײ��ϣ���ṹ��ͼ��ʾ�����й���ʯīϩ��˵����ȷ���ǣ�������| A�� | �������õĵ����� | B�� | ���ڸ߷��ӻ����� | ||
| C�� | ����ʯ��Ϊͬλ�� | D�� | ����������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=3�Ķ�Ԫ����H2R��Һ��pH=11��NaOH��Һ��Ϻ��Һ��pH����7����Ӧ��Ļ��Һ�У�2c�� R2-��+c�� HR- ��=c�� Na+ �� | |
| B�� | ij��Һ��ֻ����Cl-��OH-��NH4+��H+�������ӣ���һ�����������й�ϵ��c�� Cl- ����c�� NH4+ ����c�� H+ ��=c�� OH- �� | |
| C�� | ij���ʵ���Һ����ˮ�������c �� H+ ��=1��10-amol•L-1����a��7������Һ��pHһ��Ϊ14-a | |
| D�� | ��0.2 mol•L-1��ijһԪ��HA��Һ��0.1mol•L-1NaOH��Һ�������Ϻ���ҺpH����7����Ӧ��Ļ��Һ�У�2 c�� OH- ��+c�� A- ��=2 c�� H+ ��+c�� HA �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
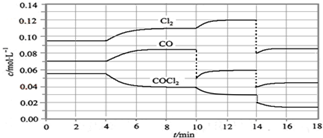
| A�� | �ӵ�10 min����12 minʱ������Cl2������v��Cl2��=0.01 mol•L-1•min-1 | |
| B�� | ��8 minʱ���18 minʱ��Ӧ��ƽ�ⳣ������ͬ | |
| C�� | �ڵ�14 minʱ���ı������������ѹ����Ӧ��������� | |
| D�� | CO��2-3min��12-13min��16-18minʱƽ����Ӧ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
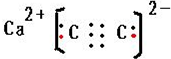 ���Ʊ���ʯ����Ҫ�õ�CaCO3�����CaCO3������Ԫ�صĵ�һ�����ܰ��Ӵ�С��˳������ΪO��C��Ca����Ԫ�ط��ţ���
���Ʊ���ʯ����Ҫ�õ�CaCO3�����CaCO3������Ԫ�صĵ�һ�����ܰ��Ӵ�С��˳������ΪO��C��Ca����Ԫ�ط��ţ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com