
【题目】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请推断后回答下列问题:
(1)Z在Y单质中燃烧的产物电子式为
用电子式表示X与R化合物的形成过程
(2)Y、Z、W、R形成的简单离子半径由大到小顺序为
(3)W单质与Z的最高价氧化物对应的水化物反应的离子方程式为
W单质与R的最高价氧化物对应的水化物反应的化学方程式为
【答案】(1)![]()
![]() (2)S2->O2->Na+>Al3+(3)2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑
(2)S2->O2->Na+>Al3+(3)2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑、2Al+3H2SO4=Al2(SO4)3+3H2↑
【解析】试题分析:X、Y、Z、W、R是五种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,则X为氢元素;Y元素原子的最外层电子数是其次外层电子数的3倍,则Y有2个电子层,最外层电子数为6,则Y为氧元素;R与Y处于同一族,则R为硫元素,Z、W、R处于同一周期,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,则Z、W原子的核外电子数之和为8+16=24,Z、W的原子序数小于R的原子序数,原子序数Z<W,Z为钠元素,W为铝元素。
(1)根据上述分析,Z为Na,Y的单质是氧气,Na在氧气中燃烧生成Na2O2,电子式为![]() ;X、R分别为H、S,H2S是共价化合物,则H2S的形成过程为
;X、R分别为H、S,H2S是共价化合物,则H2S的形成过程为![]() 。
。
(2)Y、Z、W、R形成的简单离子分别为O2-、Na+、Al3+、S2-,一般来说,电子层数越多,离子半径越大,电子层结构相同的离子,质子数越多,半径越小,则离子半径由大到小顺序为S2->O2->Na+>Al3+。
(3)W单质是Al,Z的最高价氧化物对应的水化物为NaOH,Al与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑;W单质是Al,R的最高价氧化物对应的水化物是硫酸,两者反应生成硫酸铝和氢气,反应的化学方程式为2Al+3H2SO4=Al2(SO4)3+3H2↑。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】一定条件下的密闭容器中,发生可逆反应N2 +3H22NH3。下列情况不能说明该反应一定达到化学平衡的是( )
A.NH3的质量保持不变B.H2的浓度保持不变
C.正反应和逆反应速率相等D.N2、H2、NH3的物质的量之比为1:2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体.A、B. C. D. E.F和OPA的转化关系如下所示:
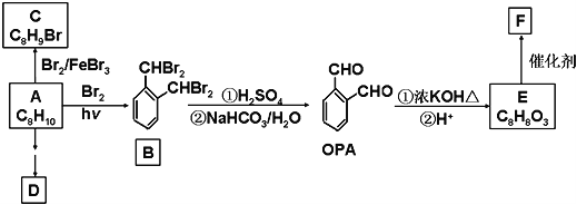
已知:
回答下列问题:
(1)A的化学名称是___;
(2)写出C所有可能的结构简式___;
(3)D(邻苯二甲酸二乙酯)是一种增塑剂。请用A. 不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D的路线___;
(4)OPA的化学名称是___,OPA经中间体E可合成一种聚酯类高分子化合物F,该反应的化学方程式为_______;
(5)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G任意一种可能的结构简式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为![]() 计算:
计算:
(1)该条件下N2的平衡转化率;(小数点后保留一位)
(2)该条件下反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数。(不带单位)
N2(g)+3H2(g)的平衡常数。(不带单位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为元素周期表截取的短周期的一部分,即![]() 。四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是
。四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是
A. 原子半径:W>Z>Y>X
B. 气态氢化物的稳定性:Z>W>X>Y
C. W的最高正化合价与负化合价的绝对值可能相等
D. Z的最高价氧化物的水化物可能为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请正确表示下列化学用语:
乙炔(结构式) ;甲烷(空间构型) ;羟基(电子式) ;
C22-(电子式) _________ ;1,3-丁二烯(实验式) 。
(2)高分子化合物![]() 是由三种单体通过加聚反应而制得的。这三种单体的结构简式是 、 、 ;
是由三种单体通过加聚反应而制得的。这三种单体的结构简式是 、 、 ;
(3)提纯下列物质(括号内为杂质)
①NaCl(KNO3)固体中提取NaCl固体: 。
②KNO3(NaCl)溶液中得KNO3固体: 。
③乙醇(水)混合物中得无水乙醇: 。
④溴苯(溴)混合物中得溴苯: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为__________________________;
(2)A中的碳原子是否都处于同一平面?____________(填“是”或“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。

(a)反应②的化学方程式为__________________________________________;
(b)C的化学名称是__________________________________________ ;
(c)E2的结构简式是__________________________________________ ;
(d)④、⑥的反应类型依次是______________________ , ____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应线路及所给信息填空。

(1)A的结构简式是 ,B的结构简式是 ;
(2)①的反应类型是 ;②的反应类型是 ;
(3)反应④的条件是 ;
(4)写出反应④的化学方程式________________ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C三种元素,已知①4 g A元素的单质与水作用,在标准状况下放出氢气2.24 L,反应中有1.204×1023个电子发生转移;②B元素可与A元素形成AB2型的离子化合物,且知A、B的离子具有相同的核外电子排布;③元素C的气态氢化物可以与其最高价氧化物对应的水化物发生非氧化还原反应生成盐,1 mol该盐含有42 mol电子。
根据以上信息填写下列空白:
(1)元素符号:A:________, B:________,C:________。
(2)A元素的离子结构示意图为____________________________________________。
(3)用电子式表示AB2的形成过程__________________________________。
(4)C的气态氢化物与B的气态氢化物反应时有___________现象发生,生成物的化学式为________,它属于________化合物。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com