
 实验法是化学重要的研究物质性质的基本方法.某化学研究小组进行了如下实验,请回答问题.
实验法是化学重要的研究物质性质的基本方法.某化学研究小组进行了如下实验,请回答问题.分析 (1)①往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来,说明过氧化钠与水反应放出热量,结合质量守恒定律可知生成NaOH和氧气,根据氧气的氧由-1价升高到0价计算转移电子数;
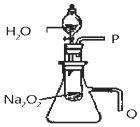
②用右图所示装置进行实验,生成氧气具有助燃性,放热使锥形瓶内气体膨胀;
(2)①光亮的无绣铁钉放入冷浓硫酸中,浓硫酸有较强的氧化性能使铁钉钝化;
②利用+2价亚铁离子能使酸化的高锰酸钾褪色来检验;乙把气体Y通入足量氯水中,生成的Y即SO2具有还原性,发生反应为:SO2+Cl2+2H2O=2HCl+H2SO4.
解答 解:(1)①往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来,可知反应生成氧气,且反应放出热量,发生的反应为2Na2O2+2H2O═4NaOH+O2↑,因为氧气的氧由-1价升高到0价,所以如果有1mol O2生成,则转移2mol 电子;故答案为:反应放出热量;2Na2O2+2H2O═4NaOH+O2↑;2;
②用右图所示装置进行实验,用以验证第二条结论的实验方法是Q导管放入盛水的水槽中有气泡产生,
故答案为:Q导管放入盛水的水槽中有气泡产生;
(2)①光亮的无绣铁钉放入冷浓硫酸中,浓硫酸有较强的氧化性能使铁钉钝化阻止反应进一步进行,故答案为:铁表面被钝化;
②a.氯水能将亚铁离子氧化为铁离子,铁离子和KSCN溶液反应导致溶液呈血红色,但不能确定原来溶液中一定含有亚铁离子,故a错误;
b.铁粉和酸反应生成亚铁离子,不能确定原来溶液中是否含有亚铁离子,故b错误;
c.浓氨水和亚铁离子反应生成氢氧化亚铁沉淀,氢氧化亚铁能被氧化生成氢氧化铁红褐色沉淀,不能确定溶液中一定含有亚铁离子,故c错误;
d.亚铁离子具有还原性,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,所以可以用酸性高锰酸钾溶液检验亚铁离子,故d正确;
乙把气体Y通入足量氯水中,生成的Y即SO2具有还原性,通入足量氯水中,发生反应为:SO2+Cl2+2H2O=2HCl+H2SO4,离子方程式为:SO2+Cl2+2H2O=4H++2Cl-+SO42-,故答案为:d;SO2+Cl2+2H2O=4H++2Cl-+SO42-.
点评 本题考查实验装置的综合及元素化合物知识,开放性较强,为高频考点,把握发生的反应、反应特点及物质的性质为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源: 题型:选择题
| A. | 混合溶液pH>7 | |
| B. | 对混合溶液进行微热,K1增大、K2减小 | |
| C. | 调节混合溶液的pH至中性,则此时溶液中c(Na+)=c(CH3COO-) | |
| D. | 温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO-)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: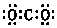 | B. | 中子数为21的钾原子:${\;}_{19}^{40}$K | ||
| C. | 甲烷分子的球棍模型: | D. | 氯离子的结构示意图: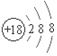 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的简单气态氢化物的热稳定性比Y的强 | |
| B. | W的氧化物的水化物的酸性一定比X的强 | |
| C. | 半径r(W)>r(Z)>r(Y)>r(X) | |
| D. | Z与Y形成的两种常见化合物中,阴、阳离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 |
| A | 将浸透了石蜡油的石棉放在大试管底部.试管中加人碎 瓷片,给碎瓷片加强热,产生的气体持续通入溴的四氯化碳溶液 | 红棕色逐渐变浅,最终褪去 |
| B | 将乙烯在空气中点燃 | 火焰呈蓝色并伴有黑烟 |
| C | 向盛有苯的试管中加入几滴酸性KMnO溶液,充分振荡 | 液体分层,溶液紫色褪去 |
| D | 将蔗糖溶液与稀硫酸混合水浴加热,取反应后的溶液少量.加人几滴新制的Cu(OH)2悬浊液加热 | 出现砖红色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中加入稀氢氧化钠溶液后,将湿润的红色试纸放在试管口 | 试纸没有变蓝色 | 溶液中不含NH4+ |
| B | 溴乙烷与NaOH溶液共热后,加HNO3酸化呈酸性,如AgNO3 | 出现淡黄色沉淀 | 溴乙烷发生了水解 |
| C | Mg(OH)2悬浊液中加入pH=7的醋酸氨溶液 | 沉淀溶解 | 加入醋酸发生NH4++OH-?NH3•H2O,使Mg(OH)2?Mg2++2OH-平衡向右移动 |
| D | 洁净的铁打在浓硝酸中浸泡片刻,蒸馏水冲洗后,再放入CuSO4溶液 | 铁定表面无红色物质生成 | 铁钉在浓硝酸中已钝化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com