
| A. | 前10min反应的平均速率v(C)=0.1 mol/(L•min) | |
| B. | 反应达到平衡时B的平衡浓度是1.5 mol•L-1 | |
| C. | 恒温下,将反应容器体积压缩为原来的一半,则D的平衡浓度小于1.0 mol•L-1 | |
| D. | 10 min后在容器中加入A,重新建立平衡时A的转化率一定大于50% |
分析 依据化学平衡三段式列式计算,反应10min后达平衡,此时D的浓度为0.5mol/L,物质的量为0.5mol/L×2L=1mol,
2A(g)+3B(g)?4C(g)+D(g)
起始量(mol) 4 6 0 0
变化量(mol) 2 3 4 1
平衡量(mol) 2 3 4 1
A、反应速率v=$\frac{△c}{△t}$计算;
B、浓度c=$\frac{n}{V}$计算;
C、反应前后气体体积不变,恒温下将反应容器体积缩小一半,压强增大,平衡不动;
D、10min后向容器中加入A,平衡正向进行,本身转化率减小;
解答 解:依据化学平衡三段式列式计算,反应10min后达平衡,此时D的浓度为0.5mol/L,物质的量为0.5mol/L×2L=1mol,
2A(g)+3B(g)?4C(g)+D(g)
起始量(mol) 4 6 0 0
变化量(mol) 2 3 4 1
平衡量(mol) 2 3 4 1
A、前10min反应的平均速率V(C)=$\frac{△c}{△t}$=$\frac{\frac{4mol}{2L}}{10min}$=0.20mol/L•min,故A错误;
B、反应达平衡时B的平衡浓度c=$\frac{n}{V}$=$\frac{3mol}{2L}$=1.5mol/L,故B正确;
C、反应前后气体体积不变,恒温下将反应容器体积缩小一半,压强增大衡不动,D的平衡浓度=$\frac{1mol}{1L}$=1.0mol/L,故C错误;
D、平衡后A转化率=$\frac{2mol}{4mol}$×100%=50%,10min后向容器中加入A,平衡正向进行,本身转化率减小,重新平衡时A的转化率一定小于50%,故D错误;
故选B
点评 本题考查了化学平衡的计算应用,主要是反应速率、转化率的计算,主要是一些化学平衡的分析判断,掌握基础是关键,题目难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
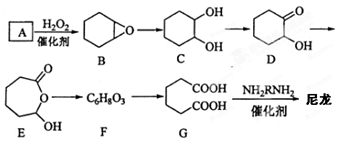
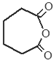 .
. .
.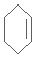 $\stackrel{Br_{2}/CCl_{4}}{→}$
$\stackrel{Br_{2}/CCl_{4}}{→}$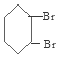 $→_{△}^{NaOH/C_{2}H_{5}OH}$
$→_{△}^{NaOH/C_{2}H_{5}OH}$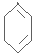 .
.查看答案和解析>>
科目:高中化学 来源:2017届安徽省黄山市高三上月考二化学卷(解析版) 题型:选择题
Cyrneine A对治疗神经系统疾病有着很好的疗效。可用香芹酮经过多步反应合成: ,下列说法不正确的是( )
,下列说法不正确的是( )
A.香芹酮的分子式为C10H14O
B.Cyrneine A可以发生加成反应、消去反应和氧化反应
C.香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色
D.与香芹酮互为同分异构体,分子中有4种不同化学环境的氢原子的酚类化合物共有3种
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
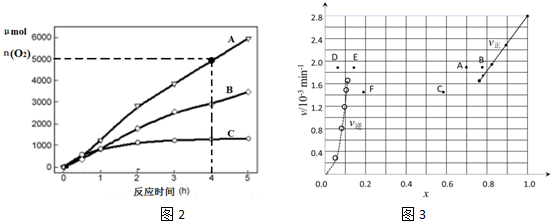
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
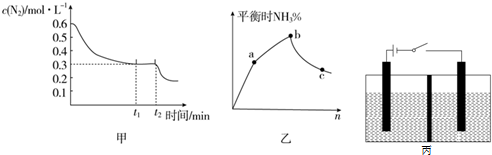
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
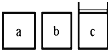 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com