
| A. | .碳酸钙的分解 | B. | .碳不完全燃烧生成CO | ||
| C. | H2在Cl2中点燃 | D. | .氢氧化钠与硝酸的反应 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 用浓氨水可以检验MgCl2、Al2(SO4)3、NaNO3溶液 | |
| B. | 用NaClO溶液检验FeSO4溶液是否变质 | |
| C. | 用盐酸和KSCN溶液检验Fe(NO3)2溶液中是否含有Fe3+ | |
| D. | 用盐酸可以检验黑色粉末氧化铜、二氧化锰、铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由①可推测溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推测溶液中一定含大量NO2- | |
| C. | 由③可推测溶液中一定含大量NO3- | |
| D. | 由实验④难以推测溶液中一定含大量SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提倡低碳生活 | B. | 大力发展私家车,减少公共交通 | ||
| C. | 利用太阳能、风能等代替化石能源 | D. | 多利用电动车和自行车 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
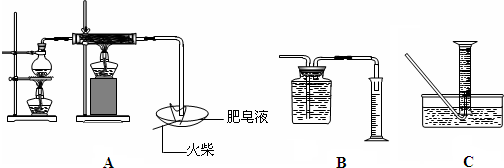
| 现象 | 结论与解释 | |
| 可能① | ||
| 可能② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
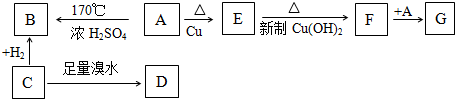
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com