
分析 (1)反应生成氯化钠和水;
(2)反应生成碳酸钙、水、二氧化碳,结合离子反应中保留化学式的物质来解答.
解答 解:(1)氢氧化钠溶液和稀盐酸反应的离子反应为OH-+H+═H2O,故答案为:OH-+H+═H2O;
(2)大理石和稀盐酸反应的离子反应为CaCO3+2H+═Ca2++H2O+CO2↑,故答案为:CaCO3+2H+═Ca2++H2O+CO2↑.
点评 本题考查了离子方程式的书写,为高频考点,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和、电子、电荷守恒等)等,题目难度不大.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题

| A. | 1molM最多可和1molNa2CO3发生反应 | |
| B. | 1molM最多可和6molH2发生加成反应 | |
| C. | 1molM最多可和3molNaOH反应 | |
| D. | 1molM最多可和2molNa反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg+2HCl═MgCl2+H2↑ | B. | 2NO+O2═2NO2 | ||
| C. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | CaCl2+Na2CO3═CaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.2g NaHSO4晶体中阳离子和阴离子的总数为0.03NA | |
| B. | 标准状况下,22.4LSO3含有NA个分子 | |
| C. | 标准状况下,11.2L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA | |
| D. | 60g石英晶体中含有的Si-O键数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | A1 | B1 | C1 | D1 |
| 电子数 | 10 | 10 | 10 | 18 |
| ② | A2 | B2 | C2 | D2 |
| 电子数 | 10 | 10 | 10 | 18 |
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
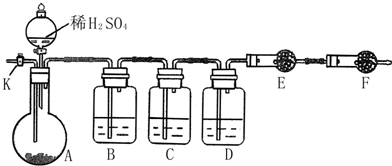
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①⑥ | C. | ②③④ | D. | ①②③⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com