
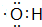 ;丙烯→A的反应类型为取代反应.
;丙烯→A的反应类型为取代反应.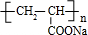 .
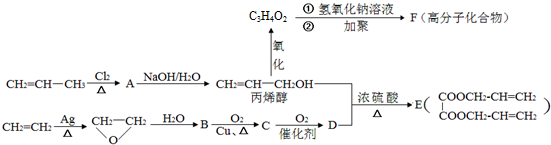
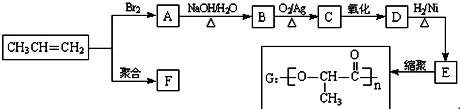
.分析 丙烯与氯气反应生成A,A发生水解反应生成CH2=CHCH2OH,则丙烯与氯气发生取代反应生成A为CH2=CHCH2Cl,烯丙醇氧化生成C3H4O2为CH2=CHCOOH,再与氢氧化反应生成CH2=CHCOONa,CH2=CHCOONa发生加聚反应生成F为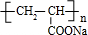 .乙烯发生氧化反应生成环氧乙烷,环氧乙烷水解生成B为HOCH2CH2OH,B反应氧化反应生成C为OHC-CHO,C进一步氧化生成D为HOOC-COOH,乙二酸与丙烯醇发生酯化反应生成E.
.乙烯发生氧化反应生成环氧乙烷,环氧乙烷水解生成B为HOCH2CH2OH,B反应氧化反应生成C为OHC-CHO,C进一步氧化生成D为HOOC-COOH,乙二酸与丙烯醇发生酯化反应生成E.
解答 解:丙烯与氯气反应生成A,A发生水解反应生成CH2=CHCH2OH,则丙烯与氯气发生取代反应生成A为CH2=CHCH2Cl,烯丙醇氧化生成C3H4O2为CH2=CHCOOH,再与氢氧化反应生成CH2=CHCOONa,CH2=CHCOONa发生加聚反应生成F为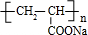 .乙烯发生氧化反应生成环氧乙烷,环氧乙烷水解生成B为HOCH2CH2OH,B反应氧化反应生成C为OHC-CHO,C进一步氧化生成D为HOOC-COOH,乙二酸与丙烯醇发生酯化反应生成E.
.乙烯发生氧化反应生成环氧乙烷,环氧乙烷水解生成B为HOCH2CH2OH,B反应氧化反应生成C为OHC-CHO,C进一步氧化生成D为HOOC-COOH,乙二酸与丙烯醇发生酯化反应生成E.
(1)B为HOCH2CH2OH,官能团为羟基,羟基的电子式为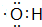 丙烯→A的反应类型为取代反应,
丙烯→A的反应类型为取代反应,
故答案为: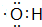 ;取代反应;
;取代反应;
(2)B→C的化学方程式:HOCH2CH2OH+O2$→_{△}^{Cu}$OHC-CHO+2H2O,
故答案为:HOCH2CH2OH+O2$→_{△}^{Cu}$OHC-CHO+2H2O;
(3)F的结构简式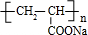 ,
,
故答案为: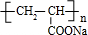 ;
;
(4)丙烯与氯气在加热条件下反应生成CH2=CHCH2Cl,然后与氯气发生加成反应生成ClCH2CHClCH2Cl,最后再氢氧化钠水溶液、加热条件下发生水解反应生成甘油(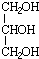 ,合成路线流程图为:CH2=CHCH3$→_{△}^{Cl_{2}}$CH2=CHCH2Cl$\stackrel{Cl_{2}}{→}$ClCH2CHClCH2Cl$→_{△}^{NaOH水溶液}$
,合成路线流程图为:CH2=CHCH3$→_{△}^{Cl_{2}}$CH2=CHCH2Cl$\stackrel{Cl_{2}}{→}$ClCH2CHClCH2Cl$→_{△}^{NaOH水溶液}$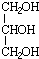 ,
,
故答案为:CH2=CHCH3$→_{△}^{Cl_{2}}$CH2=CHCH2Cl$\stackrel{Cl_{2}}{→}$ClCH2CHClCH2Cl$→_{△}^{NaOH水溶液}$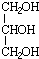 .
.
点评 本题考查有机物的推断与合成,根据有机物的结构与反应条件进行推断,熟练掌握官能团的性质与转化,是对有机化学基础的综合考查,难度中等.


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将SO2通入Ba(NO3)2溶液中,溶液变浑浊 | 生成BaSO3沉淀 |
| B | 点燃CO还原Fe2O3后的尾气,气体未能燃烧 | CO已完全反应 |
| C | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加入几滴新制氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| D | 向鸡蛋清溶液中加入少量CuSO4溶液,出现浑浊 | 蛋白质发生了盐析 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
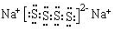 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
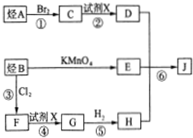
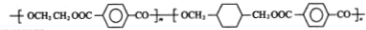
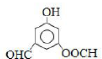 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,K+、CO32-、Br-、ClO-能大量共存 | |
| B. | 不能用稀硝酸酸化的硝酸钡溶液检验该溶液是否变质 | |
| C. | 将此溶液与稀硫酸产生的少量气体通入足量的NaAlO2溶液中制Al(OH)3:2AlO2-+SO2+3H2O═2Al(OH)3↓+SO32- | |
| D. | 能使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2H2O.
+2H2O. .
.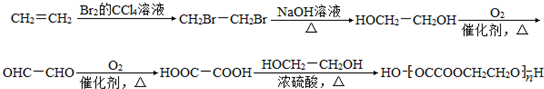 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
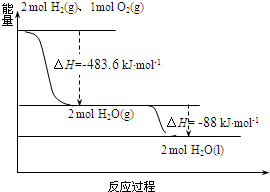
| A. | 2 mol H2(g)与1 mol O2(g)所具有的总能量比2 mol H2O(g) 所具有的总能量高 | |
| B. | 氢气燃烧的反应为放热反应,故H2与O2混合即可自发进行 | |
| C. | 液态水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=-571.6 kJ•mol-1 | |
| D. | H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度二氧化硅广泛用于制作光导纤维,其遇强碱会“断路” | |
| B. | 家用“84”消毒液可用来漂白衣物,为了增强漂白效果,可加入浓盐酸 | |
| C. | 浸泡过高锰酸钾溶液的硅藻土可以吸收乙烯,所以可用来保鲜水果 | |
| D. | 加热能杀死甲型 H1N1流感病毒是因为蛋白质受热变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com