
【题目】氢氧化镁作为水处理剂处理含Fe3+、Cr3+、Pb2+的酸性废水过程中,涉及到的化学反应类型有
A. 氧化还原反应
B. 分解反应
C. 中和反应
D. 化合反应
科目:高中化学 来源: 题型:
【题目】生活处处有化学,下列说法不正确的是
A. 过多食用糖类(如淀粉)容易使人发胖
B. 蛋白质仅含有碳、氢、氧三种元素
C. 维生素D可促进人体对钙的吸收
D. 硒是人体必需的微量元素,但不宜摄入过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A、C、E是常见的金属单质,E为紫红色,反应①可用于焊接铁轨,B是赤铁矿的主要成分,F的溶液中加入KSCN溶液变红。(部分反应物和生成物省略)

请回答下列问题:
(1)D的化学式是____。
(2)可选用____(填“字母”)实现反应C→F的转化。
a.稀盐酸 b.氯气/点燃 c.CuSO4溶液
(3)反应①的化学方程式为____。
(4)反应②的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上冶炼锡的第一步反应原理为2SnO2 + 3C ![]() 2Sn + a M↑ + CO2↑,则下列说法中错误的是
2Sn + a M↑ + CO2↑,则下列说法中错误的是
A. a的值为2 B. 反应中SnO2被还原
C. 每生成1 mol M转移电子8 mol D. 反应后有两种氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合乎实际并用于工业生产的是
A.金属钠在氯气中燃烧制氯化钠B.氢气和氯气混合经光照制氯化氢
C.氯气通入澄清石灰水中制漂白粉D.高温分解石灰石制生石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出C1O2,C1O2有类似Cl2的性质。某兴趣小组探究亚氯酸钠的制备与性质。
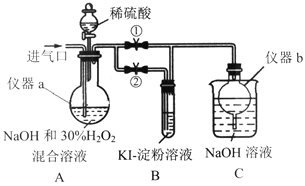
Ⅰ.制备亚氯酸钠
关闭止水夹②,打开止水夹①,从进气口通入足量C1O2,充分反应。
(1)仪器a的名称为_______,仪器b的作用是_____。
(2)装置A中生成NaC1O2的离子方程式为_______。
(3)若从装置A反应后的溶液中获得NaClO2晶体,则主要操作有减压蒸发浓缩、降温结晶______、_____干燥等。
Ⅱ.探究亚氯酸钠的性质
停止通ClO2气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸。
(4)开始时A中反应缓慢,稍后产生气体的速率急剧加快,请解释可能的原因_________。
(5)B中现象为_________ 。
(6)实验完成后,为防止装置中滞留的有毒气体污染空气,可以进行的操作是:再次打开止水夹①,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.某同学利用下列实验探究金属铝与铜盐溶液反应:
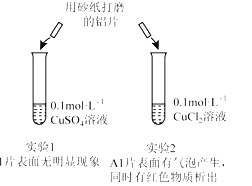
下列说法正确的是
A. 由实验1可以得出结论:金属铝的活泼性弱于金属铜
B. 溶液中阴离子种类不同是导致实验1、2出现不同现象的原因
C. 实验2中生成红色物质的离子方程式:Al+Cu2+→Al3++Cu
D. 由上述实验可推知:用砂纸打磨后的铝片分别与c(H+)均为0.2 mol/L的盐酸和硫酸反应,后者更剧烈
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com