
| A. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H>0、△S<0 | |
| B. | 滴加Cu(NO3)2溶液可以加快Zn与稀H2SO4反应制备氢气的速率 | |
| C. | 氯水中加入少量CaCO3粉末,可以提高漂白能力 | |
| D. | 化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 |
分析 A.该反应为气体体积增大的反应,△S>0,室温下不能自发进行,则△H-T△S>0;
B.滴加Cu(NO3)2溶液,酸性条件下与Zn发生氧化还原反应生成NO;
C.氯水中加入少量CaCO3粉末,碳酸钙与HCl反应,氯气与水的化学平衡正向移动;
D.平衡常数K与温度有关.
解答 解:A.该反应为气体体积增大的反应,△S>0,室温下不能自发进行,则△H-T△S>0,则该反应的△H>0,故A错误;
B.滴加Cu(NO3)2溶液,酸性条件下与Zn发生氧化还原反应生成NO,不能加快生成氢气的速率,故B错误;
C.氯水中加入少量CaCO3粉末,碳酸钙与HCl反应,氯气与水的化学平衡正向移动,HClO浓度增大,则可以提高漂白能力,故C正确;
D.平衡常数K与温度有关,与浓度、压强、催化剂无关,故D错误;
故选C.
点评 本题考查化学平衡及反应热与焓变,为高频考点,把握反应进行方向的判断、平衡移动、K与温度的关系为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各1.6 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) 2Z(g) ΔH。反应过程中测定的数据如下表:
2Z(g) ΔH。反应过程中测定的数据如下表:
t/min | 0 | 2 | 4 | 6 | 8 | … | 16 | 18 |
n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | … | … | 1.000 | 1.000 |
下列说法不正确的是
A.4—6 min时间段内Z的平均反应速率2.5×10-3 mol/(L·min)
B.该温度下此反应的平衡常数K=1.44
C.达平衡后,升高温度,K减小,则正反应△H>0
D.其他条件不变,再充入1.6 mol Z,达新平衡时Z的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:6 | B. | 6:5 | C. | 3:5 | D. | 5:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把Mg粉放入FeCl3溶液中:2Fe3++3Mg+6H2O=2Fe(OH)3↓+3 Mg2++3H2↑ | |
| B. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO?+SO2+H2O=CaSO3↓+2HClO | |
| C. | 氯化铝溶液中加入偏铝酸钠溶液:Al3++3AlO2-+6H2O=4Al(OH)3↓ | |
| D. | 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.8 mol•L-1•s-1 | D. | v (D)=1 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 中国科学家屠呦呦获拉斯克一狄贝基临床医学研究奖,以表彰她发现了一种药物--青蒿素,分子式为C15H22O5,它是由菊科植物在低温条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构筒式如图1所示.下列有关青蒿素的说法错误的是( )
中国科学家屠呦呦获拉斯克一狄贝基临床医学研究奖,以表彰她发现了一种药物--青蒿素,分子式为C15H22O5,它是由菊科植物在低温条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构筒式如图1所示.下列有关青蒿素的说法错误的是( )| A. | 青蒿素耐高温且易溶于水,不易溶于乙醚、乙酸乙酯等有机溶剂 | |
| B. | 青蒿素分子内的1个过氧基团是对付疟原虫的核心基团 | |
| C. | 提炼过程中可能用到萃取等物理方法 | |
| D. | 药效比青蒿素高10倍的双氢青蒿素(见图2)分子式为C15H24O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
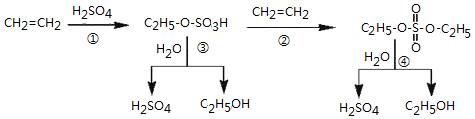
| A. | 该过程可以制取乙醇 | |
| B. | 已知C2H5-O-SO3H属于酯,所以该过程中①和②都是酯化反应 | |
| C. | 该过程中③和④是取代反应 | |
| D. | C2H5-O-SO3H具有酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com