
| A、PM2.5 |
| B、CO2 |
| C、SO2 |
| D、O3 |
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
| A、标准状况下,5LCH4气体与5LNH3气体的原子个数之比为5:4 |
| B、常温常压下,11.2LO3中所含氧原子个数大于1.5NA |
| C、同温、同压下,等体积的N2和CO气体具有相同的分子数 |
| D、室温、1标准大气压下,等质量的一氧化碳和氮气的具有相同的分子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Y2为0.2 mol/L |
| B、Y2 为0.35 mol/L |
| C、X2 为0.2 mol/L |
| D、Z为 0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(CH3COO)2 Pb+H2S=PbS↓+2 CH3COOH |
| B、Pb2++H2S=PbS↓+2H+ |
| C、Pb2++2 CH3COO-+H2S=PbS↓+2 CH3COOH |
| D、Pb2++2 CH3COO-+2H++S2-=PbS↓+2 CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三处 | B、四处 | C、五处 | D、六处 |
查看答案和解析>>
科目:高中化学 来源: 题型:
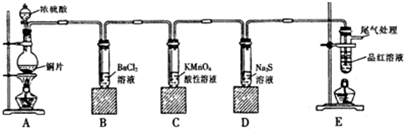
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑤ | B、②④ | C、②④⑤ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 高温高压 |
| A、使用铁触媒,可使氮气和氢气混合气体之间的反应在较低温度下取得较高的反应速率 |
| B、工业上选择上述条件下合成氨,可以使氮气全部转化为氨 |
| C、上述化学平衡的移动受到温度、反应物的浓度、压强等因素的影响 |
| D、温度升高,不利于氮气的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Ba2+、NO3-、CO32- |
| B、Ba2+、K+、Cl-、NO3- |
| C、Mg2+、NH4+、SO42-、Cl- |
| D、Fe2+、Na+、SO42-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com