
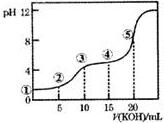
 常温下,用0.10mol•L-1的KOH标准溶液滴定10.00mL0.10mol•L-1的H2C2O4(二元弱酸)溶液所得滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1的KOH标准溶液滴定10.00mL0.10mol•L-1的H2C2O4(二元弱酸)溶液所得滴定曲线如图所示.下列说法正确的是( )| A. | 点①所示溶液中:c(H+)/c(OH-)=1012 | |
| B. | 点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| C. | 点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.1mol•L-1 | |
| D. | 点⑤所示溶液中:c(OH-)=c(H+)+c(HC2O4-)+c(H2C2O4) |
分析 A.H2C2O4为弱酸在溶液中部分电离,c(H+)<0.1mol/L;
B.H2C2O4与KOH恰好反应生成KHC2O4,溶液显酸性,说明HC2O4-的电离程度大于水解程度;
C.根据物料守恒分析;
D.氢氧化钾的物质的量是草酸的2倍,二者恰好反应而溶液呈碱性,说明草酸是二元弱酸,根据质子守恒判断.
解答 解:A.点①所示溶液中溶质为H2C2O4,H2C2O4为弱酸在溶液中部分电离,c(H+)<0.1mol/L,所以c(H+)/c(OH-)<1012,故A错误;
B.③H2C2O4与KOH恰好反应生成KHC2O4,溶液显酸性,说明HC2O4-的电离程度大于水解程度,则c(C2O42-)>c(H2C2O4),所以c(K+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4),故B错误;
C.0.10mol•L-1的KOH标准溶液滴定10.00mL0.10mol•L-1的H2C2O4(二元弱酸)溶液,由物料守恒可知,c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.1mol•L-1,故C正确;
D.⑤点时,氢氧化钾的物质的量是草酸的2倍,二者恰好反应生成草酸钠,根据质子守恒得c(H+)+c(C2O4 2- )+2c(H2C2O4)=c(OH-),故D错误;
故选C.
点评 本题考查酸碱混合溶液定性判断,明确各点溶液中溶质及其性质是解本题关键,会根据溶液酸碱性确定水解和电离程度相对大小,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒 | |
| B. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| C. | 漂白粉长期暴露在空气中会变质失效 | |
| D. | 煤炭燃烧过程安装固硫装置,可有效提高煤的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同系物:乙酸、软脂酸、硬脂酸 | B. | 同位素:氕、氘、氚 | ||
| C. | 同素异形体:金刚石、石墨、足球烯 | D. | 同分异构体:蔗糖、麦芽糖、葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 节日焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 生活中常用的塑料制品及橡胶制品都为高分子材料 | |
| C. | 向牛奶中加入果汁会产生沉淀,这是因为酸碱发生了中和反应 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
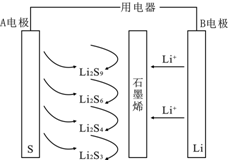 石墨烯锂硫电池放电时的工作原理示意图如图,电池反应为2Li+nS=Li2Sn,有关该电池说法正确的是( )
石墨烯锂硫电池放电时的工作原理示意图如图,电池反应为2Li+nS=Li2Sn,有关该电池说法正确的是( )| A. | 放电时,Li+向负极迁移 | |
| B. | A电极上发生的一个电极反应为:2Li++6S+2e-=Li2S6 | |
| C. | 若对该电池充电,B电极接电源正极 | |
| D. | B电极发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


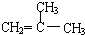 .
.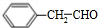 ;F分子中最多有15个原子共面.
;F分子中最多有15个原子共面.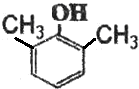 (或
(或 、
、 ).
).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B的结构简式
,B的结构简式 或
或 .
. ,反应类型:取代反应.
,反应类型:取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||||||||||||
| ⑪ | ⑫ | ||||||||||||||||
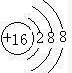 .
. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com