
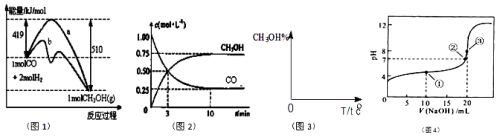
分析 (1)根据图中反应的活化能的大小来分析是否使用催化剂,利用反应前后的总能量来分析反应的能量变化;
(2)A、由图2利用转化的CO和平衡时CO的量来分析;
B、增加CO浓度,会促进氢气的转化,但本身的转化率降低;
C、该反应为反应前后压强不等的反应;
D、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动;
(3)由图2计算用CO表示的反应速率,再利用反应速率之比等于化学计量数之比来计算氢气的反应速率,利用各物质平衡的浓度来计算化学平衡常数;根据温度升高,平衡逆向移动,反应物的浓度增大,生成物的浓度减少,平衡常数减小;
(4)根据温度和压强对该反应的影响来分析;
(5)甲醇质子交换膜燃料电池,工作时将甲醇转化为甲酸,负极是甲醇失电子被氧化为甲酸,结合电荷守恒和原子守恒书写电极反应;
(6)CO的燃烧热为283kJ/mol,则CO的与氧气反应的热化学方程式为
CO(g)+$\frac{1}{2}$O2(g)═CO2(g);△H=-283kJ/mol①
H2的燃烧热为285.8kJ/mol,则H2与氧气反应的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=-285.8kJ/mol②
由图1可知,CO与H2反应可制得甲醇的热化学方程式为:CO(g)+2H2(g)═CH3OH(l);△H=-91kJ/mol③
根据盖斯定律,则CH3OH燃烧热的热化学方程式由①+②×2-③可得;
(7)点①所示溶液中,为等浓度的醋酸和醋酸钠溶液,醋酸的电离程度大于醋酸根离子的水解,溶液显示酸性.
解答 解:(1)由图可知,曲线b降低了反应所需的活化能,则b使用了催化剂,又该反应中反应物的总能量大于生成物的总能量,则该反应为放热反应,
故答案为:b;放热;
(2)A、由图2可知生成0.75mol/LCH3OH,则反应了0.75mol/LCO,平衡时有0.25mol/LCO,即CO的起始物质的量为(0.75mol/l+0.25mol/L)×2L=2mol,故A正确;
B、增加CO浓度,会促进氢气的转化,氢气的转化率增大,但CO的转化率减小,故B错误;
C、该反应为反应前后压强不等的反应,则压强不变时,该反应达到平衡状态,故C正确;
D、再充入1molCO和2molH2,体积不变,则压强增大,平衡正向移动,再次达到平衡时n(CH3OH)/n(CO)会增大,故D错误;
故答案为:AC;
(3)由图2可知,反应中减小的CO的浓度为1mol/L-0.25mol/L=0.75mol/L,10min时达到平衡,
则用CO表示的化学反应速率为$\frac{0.75mol/L}{10min}$=0.075mol•L-1•min-1,
因反应速率之比等于化学计量数之比,则v(H2)=0.075mol•L-1•min-1×2=0.15mol•L-1•min-1;
CO(g)+2H2(g)?CH3OH(g)
开始(mol/L) 1 2 0
转化(mol/L) 0.75 1.5 0.75
平衡(mol/L) 0.25 0.5 0.75
则化学平衡常数K═$\frac{0.75}{0.25×0.{5}^{2}}$L2•mol-2=12L2•mol-2;
因温度升高,平衡逆向移动,反应物的浓度增大,生成物的浓度减少,平衡常数减小;
故答案为:0.15mol•L-1•min-1;12L2•mol-2; 减小;
(4)CO(g)+2H2(g)?CH3OH(g)△H<0,
则温度越高,逆向反应进行的程度越大,甲醇的含量就越低,
压强增大,反应正向进行的程度大,则甲醇的含量高,则图象为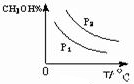 ,故答案为:
,故答案为: ;
;
(5)甲醇质子交换膜燃料电池,工作时将甲醇转化为甲酸,负极是甲醇失电子被氧化为甲酸,电极反应为:CH3OH-4e-+H2O=HCOOH+4H+,
故答案为:CH3OH-4e-+H2O=HCOOH+4H+;
(6)CO的燃烧热为283kJ/mol,则CO的与氧气反应的热化学方程式为
CO(g)+$\frac{1}{2}$O2(g)═CO2(g);△H=-283kJ/mol①
H2的燃烧热为285.8kJ/mol,则H2与氧气反应的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=-285.8kJ/mol②
由图1可知,CO与H2反应可制得甲醇的热化学方程式为:CO(g)+2H2(g)═CH3OH(l);△H=-91kJ/mol③
根据盖斯定律,则CH3OH燃烧热的热化学方程式由①+②×2-③可得:
CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l);△H=-763.6kJ/mol,
故答案为:CH3OH (g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O (l)△H=-763.6kJ/mol;
(7)点①所示溶液中,为等浓度的醋酸和醋酸钠溶液由电荷守恒可知:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),点①反应后溶液是CH3COONa与CH3COOH物质的量之比为1:1的混合物,所以c(CH3COO-)+c(CH3COOH)=2c(Na+),计算得到:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),
故答案为:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-).
点评 本题考查化学反应速率、化学平衡及能量变化,学生应注意图象的利用来分析解决问题,图象中的信息是解答本题的关键,反应热与焓变,注意盖斯定律应用,为高频考点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 某放热反应能自发进行,因此该反应是熵增反应 | |
| B. | 用惰性电极电解含有 H218O的普通水时,阳极可能产生两种相对分子质量不同的氧分子 | |
| C. | 反应 A(g)?B(g)△H,若正反应的活化能为 EakJ/mol,逆反应的活化能为 EbkJ/mol,则△H=-(Ea-Eb)kJ/mol | |
| D. | 3x%的 A 物质的溶液与 x%的 A 物质的溶液等体积混合后溶液质量分数小于 2x%,则 A 可 能为乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用图1装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用图1装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 请回答该实验中的问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某无色工业废水中可能含有Na+、Mg2+、Al3+、Cu2+、Cl-、SO42-中的几种离子.
某无色工业废水中可能含有Na+、Mg2+、Al3+、Cu2+、Cl-、SO42-中的几种离子.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
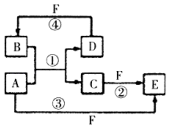 (1)短周期元素A、B、C、D、E的原子序数依次增大,A为半径最小的原子,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性,且A和E形成的化合物与A和B形成的化合物反应可产生白烟.回答下列问题:
(1)短周期元素A、B、C、D、E的原子序数依次增大,A为半径最小的原子,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性,且A和E形成的化合物与A和B形成的化合物反应可产生白烟.回答下列问题: ;
; ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O与${\;}_{8}^{16}$O是中子数相同 | B. | ${\;}_{8}^{18}$O与${\;}_{8}^{16}$O互为同位素 | ||
| C. | ${\;}_{8}^{18}$O和${\;}_{8}^{16}$O化学性质不相同 | D. | ${\;}_{8}^{18}$O和${\;}_{8}^{16}$O互为同素异形休 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
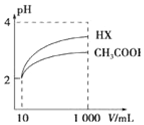 物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种.请根据所学化学知识回答下列问题:
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种.请根据所学化学知识回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
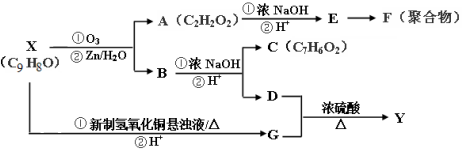
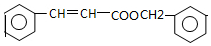 .
.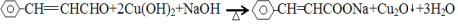 .
.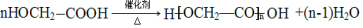 .
. .
.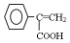 ,写出以
,写出以 为有机原料,制取H的合成路线(可任选无机原料).
为有机原料,制取H的合成路线(可任选无机原料).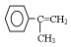 →
→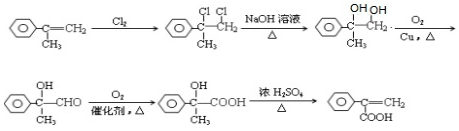 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol和9mol | B. | 2mol和9mol | C. | 3mol和9mol | D. | 3mol和6mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com