
【题目】某化学兴趣小组模拟工业上从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)中提取氧化铝的工艺做实验,流程如下:

请回答下列问题:
(1)操作Ⅰ的名称为_______。
(2)验证溶液B中是否含有Fe3+的方法:_______________________,
(3)不溶物A是___(填化学式),写出D→E反应的离子方程式______________。
(4)说出溶液F中含碳元素溶质的一种用途____________________。
【答案】过滤 取少量溶液B于试管中,加入少量KSCN溶液,若溶液变成红色,则溶液B中含有Fe3+ SiO2 AlO2-+2H2O+CO2=HCO3-+Al(OH)3↓ 发酵粉、治疗胃酸过多等
【解析】
铝土矿的主要成分是Al2O3,含SiO2、Fe2O3等杂质,由流程图可知,加足量盐酸过滤得到不溶物A为SiO2,溶液B中含Al3+、Fe3+,加过量NaOH溶液过滤得到不溶物C为Fe(OH)3,溶液D中含偏铝酸根离子,通入过量二氧化碳后过滤得到不溶物E为Al(OH)3,G为氧化铝,溶液F中含碳酸氢钠。
(1).由上述分析可知,操作I的名称为过滤,故答案为:过滤;
(2).检验溶液B中是否含有Fe3+,可选用KSCN溶液,若溶液变红色,证明含有铁离子,故答案为:取少量溶液B于试管中,加入少量KSCN溶液,若溶液变成红色,则溶液B中含有Fe3+;
(3).由上述分析可知,A为SiO2,偏铝酸钠溶液中通入过量二氧化碳反应的化学方式为NaAlO2+CO2+2H2O= Al(OH)3↓+NaHCO3,离子方程式为AlO2-+2H2O+CO2=HCO3-+Al(OH)3↓,故答案为:SiO2;AlO2-+2H2O+CO2=HCO3-+Al(OH)3↓;
(4).溶液F中含碳酸氢钠,可作发酵粉或治疗胃酸的药物等,故答案为:作发酵粉、治疗胃酸过多等。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】二氧化碳的有效回收利用,既能够缓解能源危机,又可减少温室效应的影响,具有解决能源问题及环保问题的双重意义。请回答下列问题:
(1)CO2的电子式为___________。
(2)Zn/ZnO热化学循环还原CO2制CO的原理如下图:
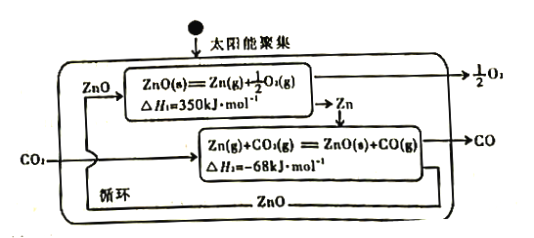
①从循环结果看,能量转化的主要方式是_________________________________。
②反应2CO2(g)=2 CO(g) +O2(g) △H=___________kJ·mol-1。
(3)二甲醚是重要的有机中间体,在一定条件下利用CO2与H2可直接合成二甲醚:
2CO2(g)+6H2(B)![]() CH3OCH3(g)+3H2O(g),当n(H2)/n(CO2)=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示。
CH3OCH3(g)+3H2O(g),当n(H2)/n(CO2)=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示。
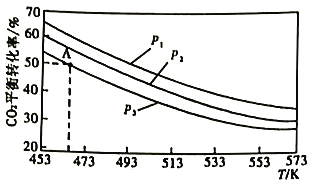
①该反应的△H___________0(填“>”或“<")。
②上图中的压强(p)由大到小的顺序为___________。
③若在1L密闭容器中充入0.2molCO2和0.6molH2,CO2的平衡转化率对应上图中的A点,则在此温度下,该反应的化学平衡常数为___________(保留整数)。
④合成二甲醚过程中往往会生成一氧化碳,合成时选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如下图所示。
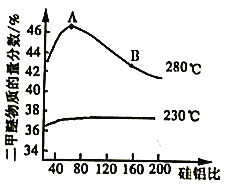
图中A点和B点的化学平衡常数比较:KA___________KB(填“>、=、<")。根据以上两条曲线,写出其中一条变化规律:____________________________________________。
(4)利用电化学原理将H2O和CO2转化为O2和燃料(C3H8O)的实验装置如下图所示。a电极的电极反应式为_________________________________。
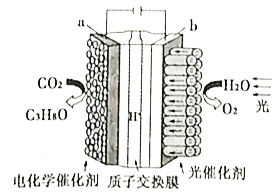 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的![]() ,发生反应
,发生反应![]() 。100℃时,体系中各物质浓度随时间变化如图所示。80s时,改变反应温度为T,
。100℃时,体系中各物质浓度随时间变化如图所示。80s时,改变反应温度为T,![]() 的浓度以
的浓度以![]() 的平均反应速率降低,经10s又达到平衡。
的平均反应速率降低,经10s又达到平衡。

完成下列填空:
(1)比较N、O的原子半径:![]() ________
________![]() (选填“
(选填“![]() ”或“
”或“![]() ”)。
”)。
(2)在0-60s时段,反应速率![]() ________
________![]() 。
。
(3)若在相同情况下最初向该容器充入的是![]() 气体,要达到上述同样的状态,
气体,要达到上述同样的状态,![]() 的起始浓度是________mol/L。
的起始浓度是________mol/L。
(4)T_____100℃(选填“![]() ”或“
”或“![]() ”),判断理由是________________。
”),判断理由是________________。
(5)画出容器在80-90s时段内![]() 和
和![]() 的浓度变化________。
的浓度变化________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙、丙分别表示在不同条件下,可逆反应A(g)+B(g)![]() xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。



(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则____曲线代表无催化剂时的情况。
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则_______曲线表示恒温恒容的情况,在该情况下混合气体中w(C)_________(填“变大”“变小”或“不变”)。
(3)根据丙可以判断该可逆反应的正反应是_____(填“放热”或“吸热”)反应,x的值为________(填范围)。
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是_________________ (填序号)。
①w(C) ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,又可作为燃料。工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-58 kJ/mol
CH3OH(g)+H2O(g) ΔH=-58 kJ/mol
③CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH=+41 kJ/mol
CO(g)+H2O(g) ΔH=+41 kJ/mol
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
化学键 | H-H | C-O | C | H-O | C-H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | x |
则x=_________。
(2)若将lmol CO2和2mol H2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应②。测得CH3OH的物质的量随时间的变化如图所示。

①曲线I、Ⅱ对应的平衡常数大小关系为KI_____KⅡ(填“>”或“=”或“<”);
②一定温度下,能判断该反应达到化学平衡状态的是_____________。
a.容器中压强不变 b.甲醇和水蒸气的体积比保持不变
c.v正(H2)=3v逆(CH3OH) d.2个C=O断裂的同时有6个H—H断裂
③若5min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率________;该温度下的平衡常数为______;若保持容器温度不变,下列措施可增加甲醇产率的________。
a.缩小反应容器的容积 b.使用合适的催化剂
c.充入He d.按原比例再充入CO2和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5。H2CO3 K1=4.5×10-7 K2= 4.7×10-11 , 草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。回答下列问题:
(1)写出水溶液中草酸的电离方程式:_____________________________________________;
(2)生活中,常用热纯碱溶液清洗油污,纯碱溶液遇酚酞显红色,请用离子方程式解释显红色的原因:________________________________________________________________;
(3)相同条件下等物质的量浓度的Na2C2O4溶液的pH比Na2CO3溶液的pH_____ (填“大”、“小”或“相等”);
(4)向1L 0.02mol/L H2C2O4溶液中滴加1L 0.01mol/L NaOH溶液。混合溶液中c(H+)>c(OH-),下列说法中正确的是(______)
A.c(H2C2O4)>c(HC2O4-) B.c(Na+)+c(H+)=2c(C2O42-)+ c(HC2O4-)+c(OH-)
C.c(OH-)= c(H+)+2c(H2C2O4)+c(HC2O4-) D.c(H2C2O4)+c(C2O42-)+c(HC2O4-)=0.02mol/L
(5)甲同学按照图所示的装置,通过实验检验草酸晶体的分解产物。装置C中可观察到的现象____________________,由此可知草酸晶体分解的产物中有__________________________。装置B的主要作用是_______________________________。

(6)设计实验证明:
①草酸的酸性比碳酸的强_________________________________________________________。
②草酸为二元酸_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ⑧ | ⑨ | ② | ③ | ||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)③、④、⑦的原子半径由大到小的顺序是________(用元素符号表示)。
(2)下列事实能说明元素②的非金属性比元素⑥的非金属性强的是________(填字母)。
A.②的单质与元素⑥的简单氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mol②单质比1mol⑥单质得电子多
C.②和⑥两元素的简单氢化物受热分解,前者的分解温度高
(3)①、②两种元素按原子个数之比为1∶1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式: ____。
(4)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式:________。
(5)已知W+X=Y+Z(反应需要加热),W、X、Y、Z分别是由①②⑨三种元素形成的四种10电子粒子(W、X为离子,Y、Z为分子),写出该离子方程式___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学常见物质且均含有同一种元素,它们之间的部分转化关系如右图所示(反应条件及其他物质已经略去):![]() 。
。
(1)若A为淡黄色固体单质,且D为强酸
①B物质通常用________________(填试剂名称)来检验。
②从组成物质的元素化合价变化角度预测B可能具有的性质_______________ ,并用相应的化学方程式表示你预测的性质_________________________________________。
③一定条件下D转化为B有多种途径,写出其中一种D→B转化的化学方程式
______________________________________________________。
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,D的稀溶液能使湿润的蓝色石蕊试纸变红。
①写出实验室制取A的化学方程式______________________________________。
②B、C都是大气污染物,它们对环境造成的危害表现在_______。
A 引起酸雨 B 引起温室效应 C形成光化学烟雾 D引起水体富营养化
③写出C→D转化的离子方程式_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com