
| A. | S的燃烧热为 297.2 kJ/mol | |
| B. | S(g)+O2(g)=SO2(g)放出的热量大于297.2 kJ | |
| C. | S(g)+O2(g)=SO2(g)放出的热量小于297.2 kJ | |
| D. | 形成1 mol SO 2中的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2(g)中的化学键所吸收的总能量 |
分析 由S(s)+O2(g)═SO2(g)△H=-297.23kJ/mol,可知该反应为放热反应,S(s)=S(g)为吸热过程,由盖斯定律可知,S(g)+O2(g)═SO2(g)△H<-297.23kJ/mol,以此来解答.
解答 解:由S(s)+O2(g)═SO2(g)△H=-297.23kJ/mol,
A.二氧化硫为稳定氧化物,S的燃烧热为297.23 kJ/mol,故A正确;
B.由盖斯定律可知,S(g)+O2(g)═SO2(g)△H<-297.23kJ/mol,则放出的热量大于297.23 kJ,故B正确;
C.由盖斯定律可知,S(g)+O2(g)═SO2(g)△H<-297.23kJ/mol,则放出的热量大于297.23 kJ,故C错误;
D.该反应为放热反应,则形成1 mol SO2的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2(g)的化学键所吸收的总能量,故D正确;
故选C.
点评 本题考查燃烧热的热化学反应方程式,明确燃烧的概念及反应热与键能、盖斯定律的计算关系即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol 过氧化钠与水反应时转移电子数为2NA | |
| B. | 16g氧气中所含的电子数为NA | |
| C. | 22.4L氯化氢溶于水可电离出1mol Cl- | |
| D. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 陶瓷、水泥和光导纤维均属于硅酸盐材料 | |
| C. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 | |
| D. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ba2+ | Ag+ | Na+ | Cu2+ |
| 阴离子 | NO3- | SO42- | OH- | CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
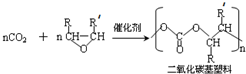 (-R、-R′代表烃基或氢原子)
(-R、-R′代表烃基或氢原子)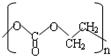 的单体是CO2和
的单体是CO2和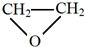 .
.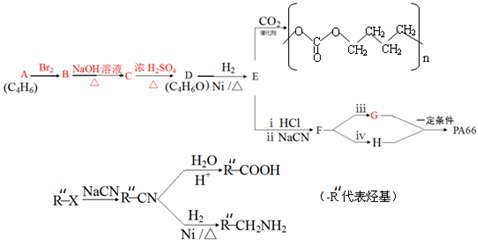
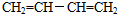 ,名称是1,3-丁二烯.
,名称是1,3-丁二烯.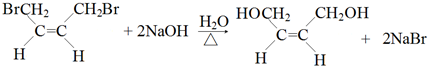 .
.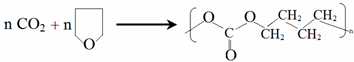 .
.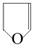 .
.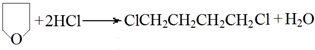 .
.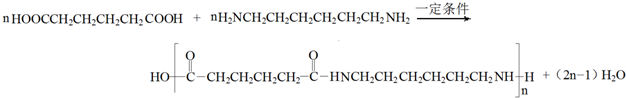 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 闻化学药品的气味时都不能使鼻子凑近药品 | |
| B. | 点燃氢气前要检查纯度,以免发生爆炸 | |
| C. | 在盛O2集气瓶中进行铁丝燃烧实验时,事先在集气瓶底铺上一层沙子 | |
| D. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于碳燃烧可能生成CO和CO2,所以碳的燃烧热大小与生成产物有关 | |
| B. | 101kPa时,2gH2完全燃烧生成液态水时放热285.8kJ,表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol,则含40.0 g NaOH的稀溶液与足量浓硫酸反应放热57.3 kJ | |
| D. | 已知C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com