
分析 (1)原电池反应是自发进行的放热的氧化还原反应;
(2)原电池反应式中,失电子化合价升高的金属单质作负极、不如负极活泼的金属或导电的非金属作正极;负极上失电子发生氧化反应、正极上得电子发生还原反应.
(3)负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应,据此书写电极反应式,然后根据电极反应式判断正极附近的pH值.
解答 解:(1)(A)中各元素化合价不变,不属于氧化还原反应,属于复分解反应,所以不能设计成原电池;
(B)中Cu元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,且该反应是放热反应、能自发进行,所以能设计成原电池,
故答案为:B;
(2)根据电池反应式知,Cu作负极,不如铜活泼的金属或导电的非金属作正极,如碳棒或银片,负极上铜失电子发生氧化反应,正极上银离子得电子发生还原反应,所以反应式分别为负极:Cu-2e-=Cu2+,正极:Ag++e-=Ag,
故答案为:Cu;Cu-2e-=Cu2+;C或Ag;Ag++e-=Ag;
(3)可燃物甲醇在负极失去电子生成二氧化碳,负极电极反应式为:CH3OH-6e-+H2O=CO2+6H+,正极氧气得到电子结合氢离子反应生成水,正极电极反应式为:4H++4e-+O2=2H2O,氢离子被消耗,所以正极附近的pH值增大,
故答案为:CH3OH-6e-+H2O=CO2+6H+;增大.
点评 本题考查原电池设计以及燃料电池的工作原理,侧重考查学生的知识运用能力,根据元素化合价的变化确定正负极,明确燃料电池中正负极上得失电子是解答(3)的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丁烷也称异丁烷 | |
| B. | 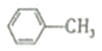 的-溴代物和 的-溴代物和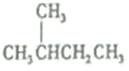 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| C. | 烷烃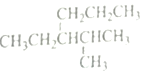 的命名是:3-异丙基己烷 的命名是:3-异丙基己烷 | |
| D. | 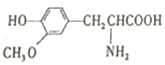 与 与 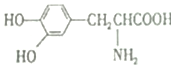 互为同系物 互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) | |
| C. | 电池工作时,溶液中的OH-由负极向正极移动 | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验步骤和装置 | |
| A | 验证SO2具有漂白性 | 将SO2通入氢氧化钠的酚酞试液中 |
| B | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
| C | 验证牺牲阳极的阴极保护法 | 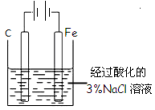 往铁电极附近滴加铁氰化钾溶液 |
| D | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的Cu(OH)2,加热3-5min. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>X>Y | |
| B. | X的单质不能与Z的氧化物反应 | |
| C. | W的单质在Y的单质中燃烧产生淡蓝色火焰 | |
| D. | X、Y可形成既有离子键又有共价键的离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化物 | B. | 硫酸盐 | C. | 硝酸盐 | D. | 碳酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ①③④ | C. | ①②③④ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com