
����Ŀ��CH4��CO2���������Եõ��ϳ�����CO��H2���������ڼ�С����ЧӦ������Ҫ��ӦΪCH4(g)+CO2(g) 2CO(g)+2H2(g) ��H��+247 kJ��mol1��ͬʱ�������·�Ӧ����̼��Ӧ��CH4(g) C(s) +2H2(g) ��H��+75 kJ��mol1����̼��Ӧ��CO2(g) +C(s) 2CO(g) ��H��+172 kJ��mol1����̼��Ӱ������Ļ��ԣ�һ��ʱ���ڻ�̼���ͷ�Ӧ�¶ȵĹ�ϵ����ͼ��

����˵����ȷ����
A.��ѹ�������CH4��ƽ��ת���ʲ����ٻ�̼
B.����CO2��CH4�����ʵ���֮�������ڼ��ٻ�̼
C.�¶ȸ���600�棬��̼��Ӧ�Ļ�ѧ��Ӧ���ʼ�������̼��Ӧ�Ļ�ѧ��Ӧ���ʼӿ죬��̼������
D.�����¶ȣ���̼��Ӧ�Ļ�ѧƽ�ⳣ��K��С����̼��Ӧ��K����
���𰸡�B
��������
A����ӦCH4(g)+CO2(g)2CO(g)+2H2(g)��CH4(g)C(s)+2H2(g)������Ӧ�������������ķ�Ӧ������ѹǿ��ƽ�������ƶ����ɼ��ٻ�̼����CH4��ƽ��ת���ʽ��ͣ���A����
B������CH4�����ʵ������䣬����CO2�����ʵ�����CO2��CH4�����ʵ���֮�������ڷ�ӦCH4(g)+CO2(g)2CO(g)+2H2(g)ƽ�������ƶ���CH4��Ũ�ȼ�С�����ڻ�̼��Ӧ��CH4(g) C(s) +2H2(g)�����ڼ���Ũ�ȼ�С��ƽ�������ƶ���̼�������٣�����CO2�����ʵ�����������̼��Ӧ��CO2(g) +C(s) 2CO(g)��ƽ�������ƶ���̼����Ҳ���٣����Ϸ���������CO2��CH4�����ʵ���֮�ȣ������ڼ��ٻ�̼����B��ȷ��
C������ͼ���¶ȸ���600�棬��̼�����٣����¶����ߣ����ڵķ�Ӧ��ϵ�з�Ӧ���ʶ��ӿ죬��C����
D��ƽ�ⳣ��ֻ���¶��йأ���̼��Ӧ����̼��Ӧ�������ȷ�Ӧ�������¶ȣ�ƽ�������ȵķ����ƶ������������ƶ���������Ӧ��ƽ�ⳣ��K������D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��Ϊ�о��绯ѧԭ���������ͼװ�á�������������ȷ����
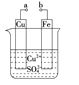
A��a��b������ʱ����Ƭ�ϻ��н���ͭ����
B��a��b�õ�������ʱ��ͭƬ�Ϸ����ķ�ӦΪ��Cu2����2e��===Cu
C������a��b�Ƿ����ӣ���Ƭ�����ܽ⣬��Һ������ɫ���dz��ɫ
D��a��b����ʱ��ͭƬ�Ϸ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤����ʵ�����Ʊ��õ���Cl2�л����HCl����ͬѧ�������ͼ��ʾ��ʵ��װ�ã���Ҫ��ش��������⡣

��1������ݼ�ͬѧ��ʾ��ͼ������ʵ��װ�ô������ҵ�����˳��װ�â���__________��
��2��װ�â�����Ҫ��������������__________��__________��__________��
��3��ʵ�����Ʊ�Cl2�����ӷ���ʽΪ____________��
��4��װ�â���Cu������__________���û�ѧ����ʽ��ʾ����
��5����ͬѧ��Ϊ��ͬѧʵ�������Ȼ����ȱ�ݣ�����֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�Ϊ�ˣ���ͬѧ�������ͨ��װ�â�֮ǰ��Ҫ��װһ������װ�âݣ���֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�����Ϊװ�â�Ӧ����__________��
��6����ͬѧ������ͬѧ��Ƶ�װ�ú����������װ�ã�ֻ�轫ԭ���ձ��е�AgNO3��Һ������ɫʯ����Һ������۲쵽__________��������֤����Cl2ʱ��HCl�ӷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ֱ��ʾ�йط�Ӧ�ķ�Ӧ�������仯�Ĺ�ϵ���ݴ��ж�����˵������ȷ���ǣ� ��
A. ʯīת��Ϊ���ʯ�����ȷ�Ӧ
B. ���ױȺ����ȶ�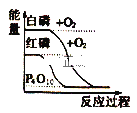
C. (g)+O2(g)=SO2(g) ��H1 S(s)+O2(g)=SO2(g) ��H2������H1>��H2
D. CO(g)+H2O(g)=CO2(g)+H2(g) ��H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤����ʵ�����Ʊ��õ���Cl2�л����HCl����ͬѧ�������ͼ��ʾ��ʵ��װ�ã���Ҫ��ش��������⡣

��1������ݼ�ͬѧ��ʾ��ͼ������ʵ��װ�ô������ҵ�����˳��װ�â���__________��
��2��װ�â�����Ҫ��������������__________��__________��__________��
��3��ʵ�����Ʊ�Cl2�����ӷ���ʽΪ____________��
��4��װ�â���Cu������__________���û�ѧ����ʽ��ʾ����
��5����ͬѧ��Ϊ��ͬѧʵ�������Ȼ����ȱ�ݣ�����֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�Ϊ�ˣ���ͬѧ�������ͨ��װ�â�֮ǰ��Ҫ��װһ������װ�âݣ���֤������ͨ��AgNO3��Һ�е�����ֻ��һ�֡�����Ϊװ�â�Ӧ����__________��
��6����ͬѧ������ͬѧ��Ƶ�װ�ú����������װ�ã�ֻ�轫ԭ���ձ��е�AgNO3��Һ������ɫʯ����Һ������۲쵽__________��������֤����Cl2ʱ��HCl�ӷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽����ȩ�����Ƶ�Cu(OH)2�ķ�Ӧ��
(1)��6 mL 6 mol��L1 NaOH��Һ�еμ�8��2%CuSO4��Һ��������0.5 mL15%��ȩ��Һ����Ͼ��ȣ�ˮԡ���ȣ�Ѹ�ٲ�����ɫ����������Χ���Ҳ�����ɫ���塣
(2)��Ӧֹͣ�����������������ó���ϴ�������Ũ���ᣬ���ܽ⡣
(3)��ͬ�����£���������Һ�����Ƶ�Cu(OH)2��Ӧ��δ�۲쵽��������
��֪��Cu2O![]() [CuCl2]����ȩ�Ǿ���ǿ��ԭ�Ե����塣
[CuCl2]����ȩ�Ǿ���ǿ��ԭ�Ե����塣
����˵����ȷ����
A.��ɫ��������Ҫ�ɷֲ���Cu2O��������Cu
B.����������ɫ����ͨ�����ȵ�CuO��õ���ɫ���壬������һ������CO
C.�Ӽ�ȩ�Ľṹ ![]() �Ʋ⣬�������������Ϊ̼�ᣨ
�Ʋ⣬�������������Ϊ̼�ᣨ![]() �������ʵ���еõ�����ɫ������CO2
�������ʵ���еõ�����ɫ������CO2
D.����-CHO���л��ﶼ���Ա�����Cu(OH)2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��д��ȷ����
A. 2SO2 + O2![]() 2SO3 ��H��-196.6 kJ��mol-1
2SO3 ��H��-196.6 kJ��mol-1
B. C(s) + O2(g) �� CO2(g) ��H��393.5 kJ��mol-1
C. H+(aq) + OH-(aq) �� H2O(l) ��H��57.3 kJ
D. ![]() H2(g) +
H2(g) + ![]() Cl2(g) �� HCl(g) ��H��-92.5 kJ��mol-1
Cl2(g) �� HCl(g) ��H��-92.5 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����Ƶļ���ԭ���װ������ͼ��ʾ���õ�ع���ʱ������˵������ȷ����
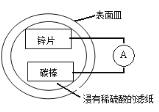
A.пƬ������
B.̼���������ݲ���
C.������пƬ����������̼��
D.�ɽ�����ת��Ϊ��ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ������������ͻ���۶���ȷ����
ѡ�� | ʵ����� | ���� | ���ͻ���� |
A | ���������Na2SiO3 ������Һ��Сľ�������ɺ���ھƾ���������� | Сľ����ȼ�� | Na2SiO3 ��������� |
B | �� H2 �ڳ���Cl2 �ļ���ƿ��ȼ�� | ����ƿ���Ϸ��а������� | H2��Cl2 ��������HCl |
C | �� SO2 ͨ�����Ը��������Һ�� | ��Һ��ɫ | SO2 ���������� |
D | ��ȥ��������Ĥ���������ھƾ����ϳ�ּ��� | �����ܵ������� | ���۵�ߣ�û���ۻ� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com