
【题目】下列离子中外层d轨道达半充满状态的是 ( )
A. 24Cr3+ B. 26Fe3+ C. 27Co3+ D. 29Cu+
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】为提高资源的利用率,可以将富锰渣(主要成分为Mn、SiO2、Al2O3、Fe)里面的锰再提炼以利用。下图为由富锰渣制备无水氯化锰的工艺流程,回答下列问题:

(1)“浸出”前将富锰渣粉碎成细颗粒,其目的是 。
(2)滤渣I的主要成分是 (填化学式)。
(3)加入MnO2氧化时,发生反应的离子方程式为 。
(4)结合下表数据(25℃),应调节pH的范围为 ,从下表中数据计算可得Al(OH)3的溶度积,该温度下Ksp[Al(OH)3]约为 。
离子 | 开始沉淀时的pH | 完全沉淀时的pH | 沉淀开始溶解时的pH |
Al3+ | 4.0 | 5.2 | 7.8 |
Mn2+ | 8.8 | 10.4 | 14 |
(5)已知MnCl2溶液呈弱酸性,操作X为 (填字母序号)。
A.蒸发结晶 B.降温结晶 C.渗析 D.盐析
(6)MnO2的生产方法之一是以惰性电极电解MnCl2和HCl混合溶液,阳极的电极反应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的“原子经济性”反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合绿色化学原理的是
A.乙烯与氧气在银催化作用下生成环氧乙烷(![]() )
)
B.乙烷与氯气制备氯乙烷
C.苯和乙醇为原料,在一定条件下生产乙苯
D.乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应为2X(g) ![]() 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:

下列推断正确的是
A.升高温度,该反应平衡常数K减小
B.压强大小为:P3>P2>P1
C.平衡后加入高效催化剂使Mr增大
D.在该条件下M点X平衡转化率为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能够达到实验目的的是( )

A.实验室采用图①所示装置收集SO2
B.可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱
C.实验室四氯化碳中常含有少量溴,加适量的苯,振荡、静置后分液,可除去四氯化碳中的溴
D.称取0.40 g NaOH,直接置于100 mL容量瓶中加水至刻度线,可配制0.10 mol/L NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定某溶液由以下离子Na+、Mg2+、Ba2+、SO42﹣、I﹣、CO32﹣中的哪几种微粒组成.进行以下实验,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是( )
A.Na+ B.SO42﹣ C.Ba2+ D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体分子中的极性键在红外线的照射下,易像弹簧一样做伸缩和弯曲运动,从而产生热量而造成温室效应。下列不属于造成温室效应气体的是( )
A.CO2 B.N2O C.CH4 D.N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷雨天闪电时空气中有臭氧生成,下列说法正确的是( )
A.O2和O3互为同位素
B.O2和O3的相互转化是物理变化
C.等物质的量的O2和O3含有相同的质子数
D.在相同的温度与压强下,等体积的O2和O3含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分) 东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_ _,提供孤电子对的成键原子是__ ___。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是____ ;氨是____ _分子(填“极性”或“非极性”),中心原子的轨道杂化类型为____。
(3)单质铜及镍都是由______键形成的晶体:元素同与镍的第二电离能分别为:I(Cu)=1959kJ/mol,I(Ni)=1753kJ/mol,I(Cu)>I(Ni)的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
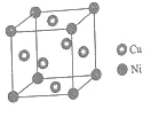
晶胞中铜原子与镍原子的数量比为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com