
| ĪļÖŹµÄĮæ/mol Ź±¼ä | n£ØN2H4£© | N£ØNO2£© | N£ØN2£© |
| ĘšŹ¼ | 2.0 | 3.0 | 0 |
| µŚ2min | 1.5 | a | 0.75 |
| µŚ4min | 1.2 | b | 1.2 |
| µŚ6min | 1.0 | c | 1.5 |
| µŚ7min | 1.0 | c | 1.5 |
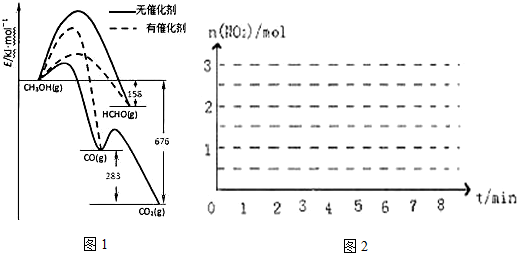
·ÖĪö £Ø1£©¢Łøł¾ŻĶ¼±ķæÉÖŖHCHO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©+H2O£Øg£©ÖŠ·“Ó¦ĪļÄÜĮæøߣ¬Éś³ÉĪļÄÜĮæµĶ£¬øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬Č»ŗóŅĄ¾ŻĶ¼ÖŠøų³öŹż¾Ż½ā“š£»
¢ŚŹ¹ÓĆ“ß»Æ¼ĮæÉŅŌ½µµĶ·“Ó¦µÄ»ī»ÆÄÜ£¬»ī»ÆÄÜŌ½µĶ£¬ĘÕĶØ·Ö×ÓŌ½ČŻŅ××Ŗ»Æ³É»ī»Æ·Ö×Ó£¬·“Ó¦Ō½ČŻŅ×£¬·“Ó¦ĖŁĀŹŌ½æģ£»
£Ø2£©¢ŁæÉÄę·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷×é·ÖµÄÅØ¶Č”¢°Ł·Öŗ¬Įæ²»ŌŁ±ä»Æ£¬¾Ż“Ė½ųŠŠÅŠ¶Ļ£»
¢Śi£®ĻČøł¾Żv=$\frac{\frac{”÷n}{V}}{”÷t}$¼ĘĖć³öĒ°2minÄŚÓĆN2H4±ķŹ¾µÄ·“Ó¦ĖŁĀŹ£¬øł¾Ż·“Ó¦ĖŁĀŹÓė»Æѧ¼ĘĮæŹż³ÉÕż±ČæÉÖŖ£ŗv£ØNO2£©=v£ØN2H4£©£»ĮŠ³öĘ½ŗā³£ŹżČż¶ĪŹ½£¬Č»ŗó½įŗĻĘ½ŗā³£ŹżµÄ±ķ“ļŹ½¼ĘĖć£»
ii£®ŅĄ¾Ż»ÆŃ§Ę½ŗāŅʶÆŌĄķ·ÖĪöŃ”Ļī£¬øıäĢõ¼ž£¬Ę½ŗāĻņ¼õČõÕāÖÖøıäµÄ·½Ļņ½ųŠŠ£¬¾Ż“Ė½ųŠŠ½ā“š£»
iii£®øł¾Ż·“Ó¦·½³ĢŹ½2N2H4£Øg£©+2NO2£Øg£©?3N2£Øg£©+4H2O£¬ĒóabcµÄֵȻŗóøł¾ŻĆčµć·Ø×÷Ķ¼£®
½ā“š ½ā£ŗ£Ø1£©¢ŁHCHO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©+H2O£Øg£©øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬”÷H=-£Ø676-158-283£©kJ•mol-1=-235kJ•mol-1£¬ĖłŅŌ1moL HCHOÉś³ÉCOµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗHCHO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©+H2O£Øg£©”÷H=-£Ø676-158-283£©kJ•mol-1=-235kJ•mol-1£¬
¹Ź“š°øĪŖ£ŗHCHO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO£Øg£©+H2O£Øg£©”÷H=-235kJ•mol-1£»
¢ŚÓÉĶ¼“߻ƼĮŹ¹Éś³ÉHCHOµÄ»ī»ÆÄܽµµĶ£¬Ķ¬Ź±Ź¹Éś³ÉCOµÄ»ī»ÆÄÜÉżøߣ¬²¢ĒŅÉś³ÉHCHOµÄ»ī»ÆÄܵĶÓŚÉś³ÉCOµÄ»ī»ÆÄÜ£¬ĖłŅŌÓŠ“߻ƼĮ×÷ÓĆĻĀ·“Ó¦£¬²śĪļÖŠHCHO±ČĀŹ“ó“óĢįøߣ¬
¹Ź“š°øĪŖ£ŗ“߻ƼĮŹ¹Éś³ÉHCHOµÄ»ī»ÆÄܽµµĶ£¬Ķ¬Ź±Ź¹Éś³ÉCOµÄ»ī»ÆÄÜÉżøߣ¬²¢ĒŅÉś³ÉHCHOµÄ»ī»ÆÄܵĶÓŚÉś³ÉCOµÄ»ī»ÆÄÜ£»
£Ø2£©¢ŁA£®»ģŗĻĘųĢåĆܶȱ£³Ö²»±ä£¬ĖµĆ÷ĘųĢåµÄÖŹĮæ²»±ä£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬“ļĘ½ŗāדĢ¬£¬¹ŹAÕżČ·£»
B.2vÕż£ØNO2£©=2vÕż£ØN2£©£¬±ķŹ¾µÄ¶¼ŹĒÕż·“Ó¦£¬ĪŽ·ØÅŠ¶ĻĘ½ŗāדĢ¬£¬¹ŹB“ķĪó£»
C£®ŅņĪŖĘšŹ¼Ź±Ķ¶ĮĻĮæÖ®±ČĪŖ1£ŗ1£¬¶ųĒŅĻūŗÄĮæŹĒ1£ŗ1£¬ĖłŅŌN2H4ÓėNO2Ģå»ż±ČŹ¼ÖÕ±£³Ö²»±ä£¬¹ŹC“ķĪó£»
D£®ĢåĻµŃ¹Ēæ±£³Ö²»±ä£¬ĖµĆ÷ĘųĢåµÄĮæ±£³Ö²»±ä£¬“ļĘ½ŗāדĢ¬£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗAD£»
¢Śi£®Ē°2minÄŚÓĆN2H4±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ£ŗv£ØN2H4£©=$\frac{\frac{2.0mol-1.5mol}{10L}}{2min}$=0.025mol•L-1•min-1£¬·“Ó¦ĖŁĀŹÓė»Æѧ¼ĘĮæŹż³ÉÕż±Č£¬Ōņv£ØNO2£©=v£ØN2H4£©=0.025mol•L-1•min-1£»
2N2H4£Øg£©+2NO2£Øg£©?3N2£Øg£©+4H2O£Øl£©
·“Ó¦Ē°£Ømol£©£ŗ2.0 3.0 0
×Ŗ»Æ £Ømol£©£ŗ1.0 1.0 1.5
Ę½ŗāŹ±£Ømol£©£ŗ1.0 2.0 1.5
øĆ·“Ó¦µÄĘ½ŗā³£ŹżK=$\frac{£Ø\frac{1.5}{10}£©^{3}}{£Ø\frac{1.0}{10}£©^{2}”Į£Ø{\frac{2.0}{10}£©}^{2}}$”Ö8.4£¬
¹Ź“š°øĪŖ£ŗ0.025mol•L-1•min-1£»8.4£»
ii£®A£®“ļµ½Ę½ŗāŹ±£¬ŅĘ×ß²æ·ÖCO2£¬Ę½ŗā½«ĻņÓŅŅĘ¶Æ£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”£¬¹ŹA“ķĪó£»
B£®øĆ·“Ó¦ŹĒĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬ĖõŠ”ČŻĘ÷µÄĢå»ż£¬Ń¹ĒæŌö“ó£¬Ę½ŗā½«ĻņÓŅŅĘ¶Æ£¬µ«c£ØN2H2£©½«Ōö“󣬹ŹBÕżČ·£»
C£®“߻ƼĮ¶ŌÕżÄę·“Ó¦ĖŁĀŹÓ°Ļģ³Ģ¶ČĻąĶ¬£¬ŌŚĻąĶ¬µÄĢõ¼žĻĀ£¬ČōŹ¹ÓĆ¼×“ß»Æ¼ĮÄÜŹ¹Õż·“Ó¦ĖŁĀŹ¼Óæģ105±¶£¬Ź¹ÓĆŅŅ“߻ƼĮÄÜŹ¹Äę·“Ó¦ĖŁĀŹ¼Óæģ108±¶£¬ŌņÓ¦øĆŃ”ÓĆŅŅ“߻ƼĮ£¬¹ŹCÕżČ·£»
D£®Čō±£³ÖĘ½ŗāŹ±µÄĪĀ¶ČŗĶŃ¹Ēæ²»±ä£¬ŌŁĻņČŻĘ÷ÖŠ³äČėHe£¬ČŻĘ÷ČŻ»żŌö“ó£¬Ń¹Ēæ¼õŠ”£¬Ę½ŗāĻņ×ÅÄęĻņŅĘ¶Æ£¬Ōņv£ØÄę£©£¾v£ØÕż£©£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗA£»
iii£®øł¾Ż·“Ó¦·½³ĢŹ½2N2H4£Øg£©+2NO2£Øg£©?3N2£Øg£©+4H2O£¬µŚ2minŹ±£¬n£ØN2H4£©=1.5mol£¬ĖłŅŌ±ä»ÆĮæĪŖ0.5mol£¬Ōņa=2.5mol£¬ÓÉ“ĖæÉĒó³öb=2.4mol£¬c=2£¬¶ųŹ¹“߻ƼĮĘ½ŗā²»ŅĘ¶Æ£»ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬ĖłŅŌ¶žŃõ»ÆµŖµÄÅØ¶Č±ä“ó£»Ōö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬ĖłŅŌ¶žŃõ»ÆµŖµÄÅØ¶Č¼õŠ”£¬ĖłŅŌĶ¼ĻóĪŖ£ŗ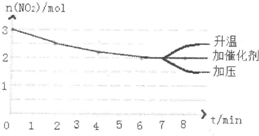 £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°»ÆŃ§Ę½ŗāµÄ¼ĘĖć”¢»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ”¢·“Ó¦ČČÓėģŹ±äµČÖŖŹ¶£¬ĢāÄæÄŃ¶Č½Ļ“ó£¬Ć÷Č·»ÆŃ§Ę½ŗā¼°ĘäÓ°ĻģĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÖŖŹ¶µć½Ļ¶ą£¬³ä·Öæ¼²éĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°×ŪŗĻÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.5 mol•L-1 | B£® | 2 mol•L-1 | C£® | 4 mol•L-1 | D£® | 5 mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó¼ü | B£® | Ēā¼ü | C£® | ¼«ŠŌ¼ü | D£® | ½šŹō¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”øßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½«ČÜÖŹµÄÖŹĮæ·ÖŹżĪŖa£„”¢ĪļÖŹµÄĮæÅضČĪŖc1 mol”¤L-1µÄĻ”ĮņĖį¼ÓČČÕō·¢µōŅ»¶ØĮæµÄĖ®£¬Ź¹ČÜÖŹµÄÖŹĮæ·ÖŹż±äĪŖ2a£„£¬“ĖŹ±ĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖc2 mol”¤L-1£¬Ōņc1ŗĶc2µÄ¹ŲĻµŹĒ£Ø £©
A£®c2=2c1 B£®c2>2c1 C£®c2<2cl D£®c1£½2c2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉżøßĪĀ¶ČŹ±£¬Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹ¼õĀż£¬Ę½ŗāÄęĻņŅĘ¶Æ | |
| B£® | Čōx=1£¬ŠĀĘ½ŗāĻĀE×Ŗ»ÆĀŹĪŖ50% | |
| C£® | Čōx=2£¬ŠĀĘ½ŗāĻĀFµÄĘ½ŗāÅضČĪŖ0.5a mol/L | |
| D£® | Čōx=2£¬»»³ÉŗćŃ¹ČŻĘ÷£¬Ōņ“ļµ½Ę½ŗāĖłŠčŹ±¼ä±ČŗćČŻČŻĘ÷ĖłŠčŹ±¼ä¶Ģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
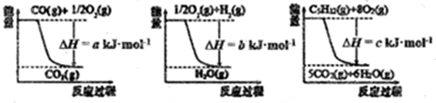
| ČŻĘ÷ | ¼× | ŅŅ | ±ū |
| ·“Ó¦ĪļĶ¶ČėĮæ | 2molH2”¢2molN2 | 4molH2”¢4molN2 | 2molNH3 |
| Ę½ŗāŹ±N2µÄÅØ¶Č£Ømol•L-1£© | c1 | 1.5 | C3 |
| N2µÄĢå»ż·ÖŹż | w 1 | w 2 | w 3 |
| »ģŗĻĘųĢåµÄĆÜ¶Č£Øg•L-1£© | ?¦Ń1 | ?¦Ń2 | ?¦Ń3? |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ČēĶ¼£¬½«4mol SO2ŗĶ2mol O2»ģŗĻĘųĢåÖĆÓŚŗćŃ¹ĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¼0£®øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬²āµĆĘųĢåµÄ×ÜĪļÖŹµÄĮæĪŖ4.2mol£®»Ų“š£ŗ
ČēĶ¼£¬½«4mol SO2ŗĶ2mol O2»ģŗĻĘųĢåÖĆÓŚŗćŃ¹ĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¼0£®øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬²āµĆĘųĢåµÄ×ÜĪļÖŹµÄĮæĪŖ4.2mol£®»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 20mL 3mol•L-1Na2S2O3µÄČÜŅŗ | B£® | 20mL 2mol•L-1Na2S2O3µÄČÜŅŗ | ||
| C£® | 10mL 4mol•L-1Na2S2O3µÄČÜŅŗ | D£® | 10mL 2mol•L-1Na2S2O3µÄČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦¢ŁÖŠ£¬Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ5 | |
| B£® | ·“Ó¦¢ŚÖŠ£¬Cu3P¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ | |
| C£® | ·“Ó¦¢ŚÖŠ£¬µ±ÓŠ5mol CuSO4·¢Éś·“Ó¦Ź±£¬¹²×ŖŅʵē×Ó10mol | |
| D£® | ·“Ó¦¢ŁÖŠCuSO4×öŃõ»Æ¼Į£¬·“Ó¦¢ŚÖŠCuSO4×÷»¹Ō¼Į |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com