
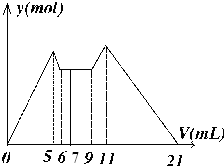
 如图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是( )
如图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是( )| A、原混合液中,C(Al3+):C(Mg2+):C(Cl-)=1:1:5 |
| B、A是NaOH,B是盐酸,且C(NaOH):C(HCl)=2:1 |
| C、从7到9,相应离子反应式H++OH-=H2O |
| D、B是盐酸,A是NaOH,且C(B)=C(A) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极反应为4OH--4e-=2H2O+O2↑ |
| B、电池放电时,电池中CO32-的物质的量将逐渐减少 |
| C、放电时CO32-向负极移动 |
| D、电路中的电子经正极、负极、熔融的K2CO3后再流回正极,形成闭合回路 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、同一主族的不同元素与另一同种元素所形成的化学式相似的物质不一定具有相同的晶体结构 |
| B、氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似的物理性质 |
| C、二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 |
| D、在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:A>B>D>C |
| B、原子序数:d>c>b>a |
| C、离子半径:C3->D->B+>A2+ |
| D、原子的最外层电子数目:A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①②④ |
| C、②④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com