
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| ①取少量滤液,滴加适量K2CO3溶液 | 有白色沉淀生成 | 滤液中含Ca(OH)2 |
| 无白色沉淀生成 | 滤液中无Ca(OH)2 | |
| ②另取少量滤液,加适量的稀盐酸 | 有无色气体逸出 | 滤液中含Na2CO3 |
| 无无色气体逸出 | 滤液中无Na2CO3 |
分析 (1)主要配料中含氯化钠,反应生成氢氧化钠,两种都易溶于水;
(2)①滤液中含有氢氧化钙,加入碳酸钾,则会出现碳酸钙白色沉淀;②Na2CO3与盐酸反应生成气体,滴加稀盐酸,有气泡产生,说明有碳酸钠,若无气体则说明没有碳酸钠;
(3)步骤①中涉及的反应是K2CO3与氢氧化钙反应生成碳酸钙沉淀,步骤②发生的反应是碳酸钠与盐酸反应生成二氧化碳气体;
解答 (1)配料中的食盐和生成的NaOH易溶于水,则滤液中肯定大量含有的溶质为NaCl和NaOH,
故答案为:NaCl、NaOH;
(2)①滤液中若含有氢氧化钙,加入碳酸钾,则会出现碳酸钙白色沉淀;②Na2CO3与盐酸反应生成气体,滴加稀盐酸,有气泡产生,说明有碳酸钠,若无气体则说明没有碳酸钠,
故答案为:Ca(OH)2;Na2CO3;
(3)步骤①中涉及的反应是K2CO3与氢氧化钙反应生成碳酸钙沉淀,反应的离子方程式为Ca2++CO32-=CaCO3↓,步骤②发生的反应是碳酸钠与盐酸反应生成二氧化碳气体,反应的离子方程式为CO32-+2H+=H2O+CO2↑,
故答案为:Ca2++CO32-=CaCO3↓;CO32-+2H+=H2O+CO2↑;
点评 本题考查元素化合物的性质以及物质的检验,题目难度不大,学习中注意把握相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 1mol白磷分子晶体中,含有的共价键为6mol | |
| B. | 离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键未被破坏 | |
| C. | 在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl- (或Na+) | |
| D. | 由于氢键作用,HF是一种非常稳定的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
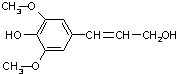 膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示.下列有关芥子醇的说法正确的是( )| A. | 芥子醇的分子式为C11H12O4,属于芳香族化合物 | |
| B. | 芥子醇分子中所有碳原子不可能在同一平面上 | |
| C. | 1mol芥子醇能与足量溴水反应消耗1molBr2 | |
| D. | 芥子醇分子中含9种不同化学环境的H原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H2SO4═2H++SO42- | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | Na2CO3═Na++CO32- | D. | Ba(OH)2═Ba+2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液的方法分离煤油和汽油 | |
| B. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉 | |
| C. | 用溶解、过滤的方法分离K2MnO4和KMnO4固体的混合物 | |
| D. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿伏伽德罗常数就是6.02×1023 mol-1 | |
| B. | 摩尔质量就是1 mol物质的质量 | |
| C. | 物质的量是衡量物质所含一定数目微观粒子集合体的物理量 | |
| D. | 物质的量的单位--摩尔只适用于微观粒子分子、原子和离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH<7的溶液一定是酸性溶液 | |
| B. | 室温时pH=5的溶液和pH=3的相比,前者c(OH-)是后者的100倍 | |
| C. | 室温下,每1×107个水分子中只有一个水分子发生电离 | |
| D. | HCl溶液中无OH-,NaCl溶液中既无OH-也无H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com