
【题目】 下列应用和相应原理(用化学方程式表示)及基本反应类型都正确的是( )
A.用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应
B.我国古代的“湿法炼铜”:2Fe+3CuSO4=3Cu+Fe2(SO4)3 置换反应
C.用天然气作燃料 CH4+2O2![]() CO2+2H2O 氧化还原反应
CO2+2H2O 氧化还原反应
D.证明金属镁的活动性比铁强:3Mg+2Fe(OH)3=3Mg(OH)2+2Fe 置换反应
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】(本题12分)可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
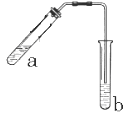
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序是:____________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是_________。
(3)实验中加热试管a的目的是:________;_________。
(4)试管b中加有饱和Na2CO3溶液,其作用是___________。
(5)反应结束后,振荡试管b,静置。反应结束后,试管B内的液体分成两层,乙酸乙酯在___层(填写“上”或“下”)。若分离10mL该液体混合物需要用到的主要玻璃仪器是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物分子中所含原子团及其数目如表.则x的值为( )
原子团 | ﹣CH2﹣ |
| ﹣CH3 | ﹣NH2 | ﹣OH |
个数 | n | m | a | 2 | X |
A.m﹣a B.n+m+a C.m+2n﹣a D.2n+3m﹣a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.MgF2晶体中的化学键是共价键
B.某物质在熔融态能导电,则该物质中一定含有离子键
C.干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力
D.N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,回答下列问题:

(1)在这些元素中:非金属性最强的元素是 ,原子半径最大的是 ,化学性质最稳定的是 (填数字序号)
(2)这些元素的最高价氧化物对应水化物中酸性最强的是 ,碱性最强的是 (填化学式)
(3)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的化学方程式为: 。
(4)呈两性的氢氧化物分别与⑤和⑦的最高价氧化物对应的水化物反应的离子方程式为 .
(5)可说明C1比S得电子能力强的是 .
①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸;③S2-比Cl-易被氧化;
④HC1比H2S稳定:⑤铜与盐酸不反应,与浓硫酸能反应。
(6)卤族元素包括F、Cl、Br等元素。下列说法正确的是 .
a.F、Cl、Br的非金属性渐弱 b.F2、Cl2、 Br2的熔点渐低 c.HF、HBr、HI的沸点渐高
(7)①、③、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案测定某品牌茶叶中钙元素的质量分数,并检验铁元素的存在(已知CaC2O4为白色沉淀物质).首先取200g茶叶样品焙烧得灰粉后进行如图操作:

请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
离子 | Ca2+ | Fe3+ |
完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的 .
(2)写出从滤液A→沉淀D的离子反应方程式 .
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试判断沉淀D已经洗涤干净的方法是 .
(4)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42﹣+2MnO4﹣+16H+═10CO2↑+2Mn2++8H2O.
现将滤液C稀释至500mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.1000molL﹣1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00mL.
①此步操作过程中需要用到图2中哪些仪器(填写序号) ;

②滴定到终点,静置后,如图3方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将 (填“偏高”“偏低”或“无影响”).
(5)原茶叶中钙元素的质量分数为 .
(6)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com