
�����������������£�����˵������ȷ���ǣ� ��
A�����ڷ�ӦnA��g��+B ��g��
 2C��g����ƽ�������ѹǿ��A�İٷֺ�����С����n��2��
2C��g����ƽ�������ѹǿ��A�İٷֺ�����С����n��2��
B�����ڷ�Ӧ2A��g��
 B��g����H��0,���º���,ѹǿ���ٱ仯˵����Ӧ�ﵽƽ��״̬��
B��g����H��0,���º���,ѹǿ���ٱ仯˵����Ӧ�ﵽƽ��״̬��
C�����ڷ�Ӧ2A��g��
 B��g�������º��������£������ܶȲ��䣬˵���ﵽƽ��״̬
B��g�������º��������£������ܶȲ��䣬˵���ﵽƽ��״̬
D�����ڷ�Ӧ2A��g��
 B��g������v��A����=2v��B������˵����Ӧ�ﵽƽ��״̬
B��g������v��A����=2v��B������˵����Ӧ�ﵽƽ��״̬

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�ɢϵ�У���ɢ�����ӵ�ֱ����10-9��l0-7 m֮�����
A��Fe(OH)3���� B���Ȼ�����Һ C������ͭ��Һ D���ཬˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���д���пո�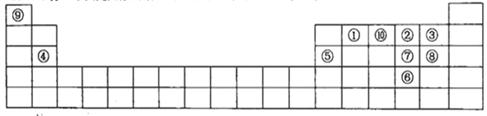
��1������10��Ԫ���У��ǽ�������ǿ����___________������ţ���
��2��Ԫ�آڢ����ԭ�Ӹ�����1:1:1�γɵĻ�������ṹʽΪ______________��Ԫ�آ�����γɵ�18e��������ĵ���ʽ____________________��
��3���ڡ��ᡢ������Ԫ���γɵĻ�����M��ԭ�Ӹ�����Ϊ3:4:2����������Ϊ42��M�к��еĻ�ѧ��������___________________________��
��4���Ƚ�Ԫ�آߢ��γɵ���̬�⻯����ȶ��ԣ�____��____���û�ѧʽ��ʾ��
��5��Ԫ�آݵ�������������������Һ��Ӧ�����ӷ���ʽ______________________��
��6��Ԫ�آܺ͢��γɵĻ��������� ������õ���ʽ��ʾ���γɹ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����(����)
A�����ۻ������ڲ������м��Լ��ͷǼ��Լ�
B��ԭ�ӻ����Ӽ�����������л�ѧ��
C���ǽ���Ԫ�ؼ�ֻ���γɹ��ۼ�
D������Ԫ����ǽ���Ԫ�ص�ԭ�Ӽ�ֻ�γ����Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��ZΪ���ֶ�����Ԫ�أ�X��Y�������ڵ��������ڣ�Xԭ�ӵ�������������Yԭ��������������2����Y��ԭ��������X��ԭ��������5��Zԭ����Yԭ�ӵ�����������֮��Ϊ3������������ȷ���ǣ�����
A. X��Y��Z����Ԫ�ز������һ����
B. X������Z����ֱ�ӷ�Ӧ���������ֻ�����
C. X��Y��Z������������Ӧ��ˮ����������ᡢ������Ե�����
D. X��Y�γɵ�һ�����Ӹ�H����Ӧ������Y������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ij�л��� ������������ȷ����(����)
������������ȷ����(����)
A��1 mol���л��������3 mol Na������Ӧ
B��1 mol���л��������3 mol NaOH������Ӧ
C��1 mol���л��������6 mol H2�����ӳɷ�Ӧ
D��1 mol���л���ֱ�������Na��NaHCO3��Ӧ����������������ͬ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij����ʽΪC10H20O2��������һ�������¿ɷ�������ͼ��ת�����̣�������������������Ľṹ����(����)
A��2�� B��4��
C��6�� D��8��
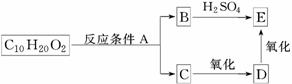
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����ԣ�Br2��Fe3+��I2������a mol FeI2����Һ�м��뺬b mol Br2����ˮ�������жϻ���Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A����a=2��b=1ʱ�����ӷ���ʽΪ��2Fe2++Br2��2Fe3++2Br��
B�������Ӧ�����Һ�д���c(Fe2+)=c(Fe3+)����4/5��a/b��1
C����a=1��b=2ʱ�����ӷ���ʽΪ��2Fe2++4I��+3Br2��2Fe3++2I2+6Br��
D����a=2��2��b��3ʱ����Һ����Ԫ��������������ʽ���ڣ���һ����c(Fe3+)��c(Fe2+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ͬʱ�����ȷ��Ӻ������ӵ��ǣ� ��
A. Һ�� B. ������ˮ C. CaCl2��Һ D. ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com