
| 周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
 .
. 分析 由元素在周期表的位置可知,A是Na,B是K,C是Mg,D是Al,E是C,F是O,G是Cl,H是Br,R是Ar.
(1)稀有气体的性质最不活泼,K的金属性最强;
(2)D元素的最高价氧化物对应的水化物与氢氧化钠,反应生成偏铝酸钠和水;
(3)电子层越多,离子半径越大,具有相同电子排布的离子中原子序数大的离子半径小;
(4)水与K反应生成KOH和氢气;
(5)非金属性越强,最高价含氧酸的酸性越强;
(6)G元素与H元素的核电荷数分别为17、35,Na的原子序数为11.
解答 解:由元素在周期表的位置可知,A是Na,B是K,C是Mg,D是Al,E是C,F是O,G是Cl,H是Br,R是Ar.
(1)这9种元素中化学性质最不活泼的是Ar,金属性最强的是K,故答案为:Ar;K;
(2)D元素的最高价氧化物对应的水化物与氢氧化钠,反应生成偏铝酸钠和水,离子反应为Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(3)A、B、C、G四种元素的简单离子半径由大到小的顺序排列为Cl->K+>Na+>Mg2+,
故答案为:Cl->K+>Na+>Mg2+;
(4)F元素氢化物的化学式是H2O,该氢化物在常温下跟B单质发生反应的离子方程式为2K+2H2O═2K++2OH-+H2↑,
故答案为:H2O;2K+2H2O═2K++2OH-+H2↑;
(5)H元素的最高价含氧酸与G的最高价含氧酸比较酸性更强的是HClO4,故答案为:HClO4;
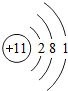
(6)G元素与H元素的核电荷数分别为17、35,二者之差为35-17=18;Na的原子序数为11,Na的原子结构示意图为 ,
,
故答案为:18; .
.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意化学用语的使用,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制硫酸亚铁溶液时,通常在溶液中加入少量的稀硫酸和铁 | |
| B. | 向BaCl2溶液中滴加稀硫酸的过程中,溶液的导电能力不变 | |
| C. | 向某溶液中加入澄清石灰水,溶液变浑浊,则该溶液一定含有CO32- | |
| D. | 把SO2通入盛有滴加了酚酞的NaOH溶液中,溶液褪色,说明SO2有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
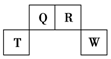 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.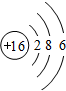 .用化学方程式表示工业常用冶炼T单质的原理是2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑.
.用化学方程式表示工业常用冶炼T单质的原理是2Al2O3(熔融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 1 | 2 | 3 | 2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4气体能与Cl2在光照条件下发生取代反应生成CCl4 | |
| B. | CH2=CH2能使酸性高锰酸钾溶液褪色是因为发生了氧化反应 | |
| C. | 通常情况下,苯是无色气体,能在催化剂条件下与Br2发生单取代反应 | |
| D. | 乙醇和乙酯发生酯化反应生成乙酸乙酯是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
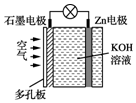
| A. | 电池放电时Zn电极逐渐溶解 | |
| B. | 石墨为正极 | |
| C. | 电子由石墨经导线流向Zn片 | |
| D. | 电池放电时实现了化学能向电能的转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时的Cu为负极 | |
| B. | 充电时电解液的pH升高 | |
| C. | 充电时阳极电极反应为:PbSO4+2H2O-2e-═PbO2+4H++SO42- | |
| D. | 每消耗1molCu,电解质溶液中转移2mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com