
分析 (1)“84”消毒液的有效成分为NaClO,另外还有较大量的Na2CO3、NaCl,通入过量的CO2,再滴入品红,发现品红很快褪色,向溶液中通入过量的CO2和次氯酸钠碳酸钠反应,与次氯酸钠溶液反应生成次氯酸和碳酸氢钠,和碳酸钠反应生成碳酸氢钠,次氯酸具有漂白性使品红褪色;
(2)①先向消毒液中加入过量的A试剂,静置后取上层清液,说明是生成了沉淀,结合“84”消毒液的有效成分为NaClO,另外还有较大量的Na2CO3、NaCl,加入试剂A是沉淀碳酸根离子,所以加入氯化钙或氯化钡溶液后得到的溶液中为氯化钠和次氯酸钠,加入硫酸,在酸溶液中发生氧化还原反应生成氯气;
②加入硫酸后生成了Cl2,该反应过程的氧化剂是HClO,还原剂是HCl,发生的反应为:NaCl+NaClO+H2SO4 =Cl2↑+Na2SO4 +H2O,每生成1mol氯气就会转移1mol电子,据此计算电子转移;
解答 解:(1)“84”消毒液的有效成分为NaClO,向溶液中通入过量的CO2时反应的基本原理是强酸制弱酸,所以发生的两个离子方程式是:ClO-+CO2+H2O=HClO+HCO3-,还有较大量的Na2CO3,该反应是碳酸钠和转化成碳酸氢钠的过程,H2O+CO2+CO32-=2HCO3-,
故答案为:ClO-+CO2+H2O=HClO+HCO3-,H2O+CO2+CO32-=2HCO3-;
(2)①以该消毒液为主要来源可以制备较纯净的少量Cl2,具体操作分两个主要步骤:先向消毒液中加入过量的CaCl2或者BaCl2试剂,除去CO32-,
故答案为:CaCl2或者BaCl2,除去CO32-离子;
②静置后取上层清液,再加入了硫酸,加入硫酸后生成了Cl2,该反应过程的氧化剂是HClO元素化合价+1价变化为0价,还原剂是HCl元素化合价-1价变化为0价,发生的反应为:NaCl+NaClO+H2SO4 =Cl2↑+Na2SO4 +H2O,具体的计算出过程如下:NaCl+NaClO+H2SO4 =Cl2↑+Na2SO4 +H2O,每生成1mol氯气就会转移1mol电子,所以由,2.8L氯气得到氯气的物质的量=$\frac{2.8L}{22.4L/mol}$=0.125mol,所以转移的电子数是0.125mol×NA=0.125NA,
故答案为:HClO;HCl;0.125NA;
点评 本题考查了次氯酸是漂白性 物质的量的计算,能用所学的知识解决实际问题是学生必须要达到的目标,所以此类题目主要考查学生对所学知识的熟练运用能力,题目难度中等.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 3 mL | B. | 7.5 mL | C. | 15 mL | D. | 22.5 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2Mn2O7→4NaMnO4+O2↑ | B. | 2Na2O2+P2O3→Na4P2O7 | ||
| C. | 2Na2O2+2 N2O3→NaNO2+O2↑ | D. | 2 Na2O2+2 N2O5→4NaNO3+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
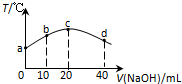 常温下,若往20mL 0.01mol•L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )
常温下,若往20mL 0.01mol•L-1 HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( )| A. | HNO2的电离平衡常数:c点>b点 | |
| B. | 所加烧碱溶液PH=12,c点水的离子积常数KW=10-14 | |
| C. | c点混合溶液中:c(OH-)>c(HNO2) | |
| D. | d点混合溶液中:c(Na+)>c(OH-)>c(NO2-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂与方法 | 原理 |
| A | 灭火 | 混合Al2(SO4)3与NaHCO3两种溶液 | 两物质直接发生化学反应产生CO2 |
| B | 制备胆矾 | 将CuSO4溶液加热直至蒸干 | 加热促进Cu2+的水解 |
| C | 配制AlCl3溶液 | AlCl3溶液中加硫酸 | 抑制Al3+水解 |
| D | 除铁锈 | NH4Cl溶液 | NH4Cl溶液显酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com