
【题目】下列各组离子能在呈酸性的无色溶液中大量共存的是( )
A. Ba2+、Na+、NO3-、MnO4- B. Mg2+、Cl-、Al3+、SO42-
C. K+、Na+、CO32-、NO3- D. Ca2+、NO3-、Fe3+、Cl-
科目:高中化学 来源: 题型:
【题目】关于原电池和电解池的叙述正确的是( )
A. 原电池中失去电子的电极为阴极
B. 原电池的负极、电解池的阳极都发生氧化反应
C. 原电池的两极一定是由活动性不同的两种金属组成
D. 电解时电解池的阴极一定是阴离子放电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中错误的是
A.构成原电池的正极和负极必须是两种不同的金属
B.原电池是将化学能转变为电能的装置
C.在原电池中,电子流出的一极是负极,发生氧化反应
D.原电池放电时,电流的方向是从正极经导线到负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2

某化学兴趣小组将上述流程②③设计成如下图所示操作。
回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①_____________ ③_____________
(2)F中下层液体的颜色为_____色,上层液体中溶质的主要成分为_____。(填化学式)
(3)在灼烧过程中,使用到的实验仪器有(除泥三角外)_______________(填序号)。
①试管 ②坩埚 ③坩埚钳 ④蒸发皿 ⑤酒精灯
(4)为获取晶体碘,该兴趣小组设计如下两个装置图:
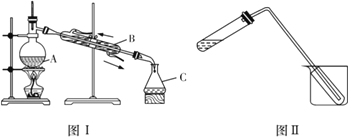
①图Ⅰ中仪器A、C的名称分别是________、________。该装置中的错误之处为___________。
②实验时仪器A中除加入一定量碘有机溶液外,还需加入少量________,其作用是_________ 。
③图Ⅱ装置可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图Ⅰ完全相同。该装置中使用的玻璃导管较长,其作用是_________;烧杯中还应盛有的物质是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)与16g氧气所含原子总数相同的氨气是_____________g;在相同条件下,在5.6g氮气中应添加___________g氨气所组成的混合气体与16g氧气所占的体积相等。
(2)把__________g NaOH溶解在90g水中,才能使得每10个水分子中有1个Na+。
(3)质量之比为16∶7∶6的三种气体SO2、CO、NO,氧原子个数之比为________。
(4)某气体氧化物的化学式为RO2,在标准状况下,0.92g该氧化物的体积为448mL,则该氧化物的摩尔质量为________。
(5)8.5g氢氧根离子含有的电子数目为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.常温下,在0.1mol·L-1的HNO3溶液中,由水电离出的c(H+)<![]()
B.浓度为0.1mol·L-1的NaHCO3溶液:c(H2CO3)>c(CO32-)
C.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
D.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓H2SO4(密度为1.84 g/mL)配制1 mol·L-1的稀H2SO4100mL,配制过程中可能用到下列仪器:
①100mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤100mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用出现的先后顺序排列正确的是
A. ②⑥③⑦⑤ B. ④③⑤⑦⑥ C. ①③⑦⑤⑥ D. ②⑤⑦⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
2CO(g)+2NO(g)![]() 2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH2=-565kJ·mol-1
(1)在一定条件下N2和O2会转化为NO,写出该反应的热化学方程式:_________。
(2)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.4mol CO,在催化剂存在的条件下发生反应,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后n(CO)=________mol,关于该平衡的下列说法正确的是________。
a.增大压强,平衡一定向右移动
b.其他条件不变,升高温度,化学反应速率一定增大
c.其他条件不变,若改为在恒压容器中进行,CO的平衡转化率比恒容条件下大
d.达到平衡后v正(NO)=2v逆(N2)
(3)其他条件相同,t min时不同温度下测得NO的转化率如图所示。

A点的反应速度v正________(填“>”、“<”或“=”)v逆,A、B两点反应的平衡常数较大的是________(填“A”或“B”)。
(4)已知HNO2的电离常数Ka=7.1×10-4mol·L-1;
NH3·H2O的电离常数Kb=1.7×10-5mol·L-1
则0.1mol·L-1NH4NO2溶液中离子浓度由大到小的顺序是____________________________,
常温下NO2-水解反应的平衡常数Kh=________(保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com