
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
下列说法不正确的是
A.焓变是判定一个反应能否自发进行的相关因素,多数放热反应能自发进行
B.在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大
C.自发进行的反应一定能迅速进行
D.一个反应能否自发进行,与焓变和熵变的共同影响有关
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上月考化学试卷(解析版) 题型:填空题
(除标注外,每空2分,共8分)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产NiOOH的一种工艺流程如下:

(1)加入Na2CO3溶液时,确认Ni2+已经完全沉淀的实验方法是__ __。
(2)已知Ksp[Ni(OH)2]=2×10-15,欲使NiSO4溶液中残留c(Ni2+)≤2×10-5 mol·L-1,调节pH的范围是__ _。
(3)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式:
____。
(4)若加热不充分,制得的NiOOH中会混有Ni(OH)2,其组成可表示为xNiOOH·yNi(OH)2。现称取9.18 g样品溶于稀硫酸,加入100 mL 1.0 mol·L-1 Fe2+标准溶液,搅拌至溶液清亮,定容至200 mL。取出20.00 mL,用0.010 mol·L-1 KMnO4标准溶液滴定,用去KMnO4标准溶液20.00 mL,试通过计算确定x、y的值。涉及反应如下(均未配平):
NiOOH+Fe2++H+——Ni2++Fe3++H2O
Fe2++MnO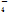 +H+——Fe3++Mn2++H2O
+H+——Fe3++Mn2++H2O
则x=____;y=__。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省普宁市高一上学期第三次月考化学试卷(解析版) 题型:实验题
下图为两套实验装置。
(1)写出下列仪器的名称:
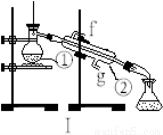
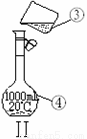
① ;② 。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填序号)
(3)若利用装置I制取蒸馏水,还缺少的仪器是 ,将仪器补充完整后进行实验,冷却水从 口进。
(4)现需配制1.0 mol·L-1的NaOH溶液240mL,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误分别是 、 。
(5)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为_____________________。
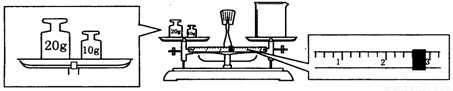
(6)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为______g,该同学应称量______g NaOH。
(7)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏高的是__________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量溶液洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省普宁市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列反应中的氨与反应4NH3+5O2=4NO+6H2O中的氨作用相同的是
A. 2Na+2NH3=2NaNH2+H2↑ B. 2NH3+3CuO=3Cu+N2+3H2O
C. NH3+H2O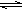 NH3·H2O D. HCl+NH3=NH4Cl
NH3·H2O D. HCl+NH3=NH4Cl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
现有0.05mol·L-1 CH3COOH溶液500 mL,若加500 mL水或加入部分CH3COONa晶体时,都会引起
A.溶液的pH增大 B.CH3COOH的电离程度增大
C.溶液的导电能力减小 D.溶液的c (OH – )减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH = -221 kJ·mol-1 ,②稀溶液中,H+(aq)+OH-(aq) =H2O(l) ΔH = -57.3 kJ·mol-1。由此可以推断下列结论正确的是
A.稀硫酸与稀氨水溶液反应生成1 mol水,放出57.3 kJ热量
B.①的焓变为221 kJ·mol-1
C.浓硫酸与稀NaOH溶液完全反应生成1 mol水时放热为57.3 kJ
D.1mol碳完全燃烧放出的热大于110.5 kJ
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市高一上学期期中测试化学试卷(解析版) 题型:填空题
将27.4g Na2CO3和NaHCO3的混合物平均分成等量的两份,一份溶于水后加入足量某浓度的盐酸恰好完全反应,收集到CO2气体V L ,消耗盐酸100 mL。另一份直接加热至恒重,生成CO2气体1.12 L(所有气体体积均在标准状况下测定)。试计算:
(1)原混合固体中Na2CO3和NaHCO3的物质的量之比:n(Na2CO3):n(NaHCO3)=____________;
(2)盐酸的物质的量浓度c(HCl)=______________mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中考试化学试卷(解析版) 题型:填空题
选择下列一种方法分离物质,将分离方法的序号填在横线上.
A萃取 B升华 C结晶 D分液 E蒸馏 F过滤
(1)从溴水中提取溴_________
(2)从含有少量氯化钾的硝酸钾混合液中获得硝酸钾_________
(3)分离水和汽油的混合物_________
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)两种互溶液体_________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com