
废气中的H2S通过高温热分解可制取氢气:2H2S(g) 2H2(g)+S2(g)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
2H2(g)+S2(g)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
(1)某温度时,测得反应体系中有气体1.3lmol,反应1 min后,测得气体为l.37mol,则tmin 内H2的生成速率为___________。
(2)某温度时,H2S的转化率达到最大值的依据是_____________(选填编号)。
a.气体的压强不发生变化 b.气体的密度不发生变化
c. 不发生变化 d.单位时间里分解的H2S和生成的H2一样多
不发生变化 d.单位时间里分解的H2S和生成的H2一样多
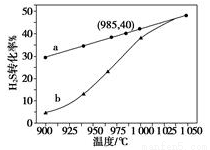
(3)实验结果如下图。图中曲线a表示H2S的平衡转化率与温度关系,曲线b表示不同温度下、反应经过相同时间且未达到化学平衡时H2S的转化率。该反应为_____反应(填“放热”或“吸热”)。曲线b随温度的升高,向曲线a通近的原因是_________。在容器体积不变的情况下,如果要提高H2的体积分数,可采取的一种措施是________。
(4)使1LH2S与20L空气(空气中O2体积分数为0.2)完全反应后恢复到室温,混合气体的体积是______L 。若2gH2S完全燃烧后生成二氧化硫和水蒸气,同时放出29.4 kJ的热量,该反应的热化学方程式是__________________。
科目:高中化学 来源:2017届湖北省八校高三第二次联考(3月)理综化学试卷(解析版) 题型:选择题
分子式为C4H8O的三元环同分异构体共有(不考虑立体异构)( )
A. 5种 B. 6种 C. 7种 D. 8种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高一3月月考化学试卷(解析版) 题型:选择题
X、Y、Z为短周期元素,原子序数依次增大。X原子最外层电子数是Y原子最外层电子数的2倍,质子数比Y少5,X和Z在同一主族。下列叙述不正确的是 ( )
A. 原子半径:Y>Z
B. X元素的一种单质可用于消毒杀菌
C. Y的单质在空气中放置表面 易生成一层致密的氧化膜
易生成一层致密的氧化膜
D. Z的单质在氧气中点燃可生成两种酸性氧化物
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三第五次摸底考试理综化学试卷(解析版) 题型:简答题
Ⅰ.高纯度氢氧化镁广泛应用于医药、电力等领域。镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如图所示:
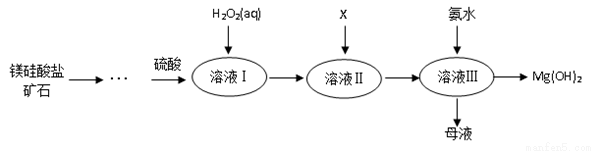
已知:
①溶液Ⅰ中除含Mg2+、SO42?外,还含有少量Fe3+、Al3+、Fe2+等离子;
②常温下,几种金属离子开始沉淀和沉淀完全时的pH如下表所示:
金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
开始沉淀时的pH | 1.5 | 3.3 | 6.5 | 9.4 |
沉淀完全时的pH | 3.7 | 5.2 | 9.7 | 12.4 |
请回答下列问题:
(1)镁在元素周期表中的位置_______________;
(2)向溶液Ⅱ中加入试剂X是_____________,作用是_________________________;
(3)流程中不加H2O2引起的后果是___________________________________;
(4)说出母液的一种用途___________________;
(5)加入H2O2溶液发生反应的离子方程式是___________________;
Ⅱ.海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
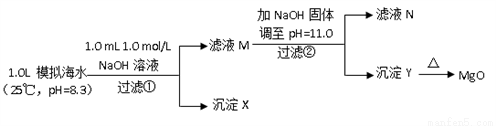
模拟海水中的离子浓度/ (mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp [Ca(OH)2]=4.68×10-6;Ksp [Mg(OH)2]=5.61×10-12。请回答下列问题:
(6)沉淀物X为_____________;
(7)滤液N中Ca2+浓度为_______________;
(8)加NaO H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
H固体调整pH=12.5是否可行______(填“是”“否”);原因是________。
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三第五次摸底考试理综化学试卷(解析版) 题型:选择题
a、b、c、d为短周期元素,a的原子中只有1个电子,b与a可形成多种有机化合物,c的单质是构成空气的主要成分,d元素的焰色反应呈黄色。下列叙述错误的是
A. 简单离子半径:c>d
B. a、b、c、d中,d的原子半径最大
C. a与b、c形成的化合物可能含有非极性键
D. a与其它元素形成的化合物均为共价化合物
查看答案和解析>>
科目:高中化学 来源:2017届上海市普陀区高三第二学期质量调研(二模)化学试卷(解析版) 题型:选择题
向0.lmol/LCH3COOH溶液中加入少量Na0H固体(忽略温度、体积变化),增大的是
A. 氢离子浓度 B. 水的电离程度 C. 水的离子积 D. 醋酸浓度
查看答案和解析>>
科目:高中化学 来源:2017届上海市普陀区高三第二学期质量调研(二模)化学试卷(解析版) 题型:选择题
短周期元素W、Q、X、Y在元素周期表中的位置如右图,其中X是两性金属元素。则

A. 简单离子半径:X<Q B. 气态氢化物的稳定性:Y>Q
C. X的族序数大于周期数 D. Y氧化物对应水化物是强酸
查看答案和解析>>
科目:高中化学 来源:2017届山西省太原市高三模拟考试(一)理综化学试卷(解析版) 题型:选择题
我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S,已知甲池中发生的反应:
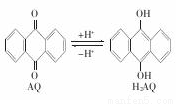
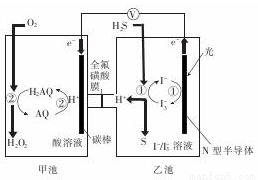
下列说法正确的是( )
A. 甲池中碳棒上发生的电极反应为AQ+2H+-2e-=H2AQ
B. 乙池溶液中发生的反应为H2S+I3-=3I-+S+2H+
C. 该装置中电能转化为光能
D. H+从甲池移向乙池
查看答案和解析>>
科目:高中化学 来源:宁夏勤行校区2016-2017学年高二下学期第一次(3月)月考化学试卷 题型:简答题
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
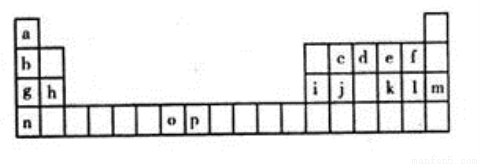
(1)写出元素k的基态原子的电子排布式________________________________,其原子核外有________个未成对电子。
(2)单质c在空气中充分燃烧的产物的分子构型为________ ,中心原子的杂化方式为_______,该分子含有________(填“极性键”或“非极性键”), 该分子是________分子(填“极性”或“非极性”)。
(3)上述元素的最高价氧化物的水化物中,酸性最强的是___________________,碱性最的___________________(填化学式)。(每空1分)
(4)d的气态氢化物与d的最高价氧化物的水化物反应的离子方程式是:___________________________________________________________________________________________________________________________________。
(5)o、p两元素的部分电离能数据列于下表:比较两元素的I2、I3可知,气态o2+再失去一个电子比气p2+再失去一个电子困难。对此,你的解是__________________________________________________________________________。
元素 | o | P | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
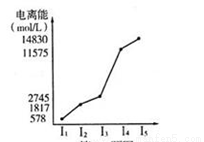
(6)短周期某主族元素的电离能情况如上图所示,则元素是上述周期表的__________元素(填元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com