
����Ŀ�������£�������������Һ��
�� | �� | �� | �� | �� |
0.1 mol��L-1 CH3COOH��Һ | 0.01mol��L-1 CH3COOH��Һ | pH��2 CH3COOH��Һ | 0.1 mol��L-1 NaOH��Һ | 0.1mol��L-1 ��ˮ |
�ش��������⣺
��1����Һ��ϡ�͵�ԭ����10�������ҺpH______����Һ��pH������������������������������ͬ�����ٺ͢�����Һ��ˮ�������c(H��)����_______��
��2������ͬ�¶�ʱ100mL �ڵ���Һ��10mL �ٵ���Һ��Ƚϣ�������ֵǰ�ߴ��ں��ߵ���_______
A �к�ʱ����NaOH���� B ����̶�
C ˮ�������c(H��) D CH3COOH�����ʵ���
��3����ˮϡ�͢�ʱ����Һ������ˮ�������Ӷ���С����______������ĸ����
A��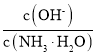 �������������� B��
�������������� B��
C��c��H+����c��OH-���ij˻���������D�� OH-�����ʵ���
��4��������N2H4������ˮ�Լ��ԣ���ԭ���백���ƣ�������Բ��簱ǿ��д��������ˮ�ʼ��Ե����ӷ���ʽ��________��
���𰸡��� �� BC B N2H4+H2O![]() N2H5+ +OH-
N2H5+ +OH-
��������
��1���ٵ�Ũ��Ϊ0.1mol/L��pH=2��CH3COOH��Һ��Ũ�ȴ���0.01mol/L��ϡ�͵�ԭ����10�����۵�������Ũ�ȴٺ͢�����Һ��ˮ�ĵ������������ã������ӻ�����������Ũ��Խ���ˮ�ĵ�������Ƴ̶�Խ��ˮ�������c��H+��ԽС��
��2������ͬ�¶�ʱ��100mL�ڵ���Һ��10mL�ٵ���Һ��Ƚϣ�
A������Һ�д�������ʵ�����ͬ���к�ʱ����NaOH������ȣ�
B��ԽϡԽ���룻
C��������Һ��������Ũ�ȴ���ǰ�ߣ�����ˮ�������c��H+��ǰ�ߴ��ں��ߣ�
D��CH3COOH�����ʵ�������Ϊǰ�ߵĵ���̶ȴ��ں��ߣ�����CH3COOH�����ʵ���ǰ��С�ں��ߣ�
��3����ˮ�ٽ���ˮ�ĵ��룬n��OH-�����n��NH3H2O����С����
A�� �൱��
�൱�� ���
���
B�� �൱
�൱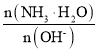 �ڼ�С��
�ڼ�С��
C���¶Ȳ��䣬����c��H+����c��OH-���ij˻����䣻
D��OH-�����ʵ������
��4���������Ӧ�ã�������ˮ�ķ�Ӧ�����ʣ�������һ����ɫ��ȼ��Һ�壬����ˮ�Լ��ԣ���ԭ���백���ƣ������� NH3+H2O![]() NH4++OH-���Է�����������ˮ��Ӧ�ķ���ʽ��
NH4++OH-���Է�����������ˮ��Ӧ�ķ���ʽ��
��1����CH3COOH��Һ��Ũ��Ϊ0.1mol/L��ϡ�͵�ԭ����10����Ũ�ȱ�Ϊ0.01 mol��L-1�����ڴ��������ᣬ����ȫ���룬������PH��2��0.1 mol��L-1CH3COOH��Һ�е�c(H+)С��0.1 mol��L-1NaOH��Һ�е�c(OH-)������ˮ����������ӵ�Ũ�Ȣ٣��ڣ��ʴ�Ϊ����������
��2������ͬ�¶�ʱ��100mL ��0.01mol��L-1 CH3COOH��Һ��10mL ��0.1 mol��L-1CH3COOH��Һ��Ƚϣ�
A������Һ�����ʵ����ʵ�����ͬ���к�ʱ����NaOH������ȣ��ʲ�ѡ��
B��ԽϡԽ���룬����̶�Խ��ѡ��
C��������Һ��������Ũ�ȴ���ǰ�ߣ�����ˮ�������c��H+��ǰ�ߴ��ں��ߣ���ѡ��
D��CH3COOH�����ʵ�������Ϊǰ�ߵĵ���̶ȴ��ں��ߣ�����CH3COOH�����ʵ���ǰ��С�ں��ߣ��ʲ�ѡ��
��ѡBC��
��3��A�� �൱��
�൱�� ���
���
B�� �൱��
�൱��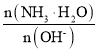 ��С��
����
C���¶Ȳ��䣬����c��H+����c��OH-���ij˻����䣻
D��OH-�����ʵ������ѡB��
��4����������ˮ�Լ��ԣ���ԭ���백���Ƽ�N2H4+H2O![]() NH2NH3++OH-����һ����ӦҲ����ΪNH2NH3++H2O
NH2NH3++OH-����һ����ӦҲ����ΪNH2NH3++H2O![]() NH3NH32++OH-��
NH3NH32++OH-��


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��ijѧ����0.100molL-1��KOH����Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷֽ�Ϊ���¼�����
A���ñ���Һ��ϴ�ζ���2��3�Σ�
B��ȡ��KOH��Һע���ʽ�ζ������̶���0������2��3cm ����
C����ʢ�б���Һ�ļ�ʽ�ζ��̶ܹ��ã����ڵζ���ʹ���촦������Һ��
D������Һ������0������0�����¿̶ȣ����¶�����
E����ȡ20mL����������Һע��ྻ����ƿ�У�������2��3�η�̪��
F������ƿ���ڵζ��ܵ����棬�ñ�KOH��Һ�ζ����յ㲢���µζ���Һ��Ŀ̶ȡ�
ʵ���� | KOH��Һ��Ũ��(mol/L�� | �ζ����ʱ��KOH��Һ����������mL�� | ����������Һ�������mL�� |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
�ʹ�ʵ�������գ������������ݣ��ɼ�����������Ũ��ԼΪ__________��������λ��Ч���֣�
II������������һ�ֳ���ʳƷ���Ӽ���Ϊ����ijʳƷ���������κ���(ͨ����1kg��Ʒ�к�SO2��������)��ij�о�С��������������ԭ�ζ��������вⶨ��ʵ���������£�

��1�����ҺӦѡ��____(������ʽ��������ʽ��)�ζ���ʢװ����ע��Һ֮ǰ����Եζ��ܽ���_____��ϴ�ӡ�____��
��2����ƿ�ڵ�ָʾ��Ϊ_____���жϴﵽ�ζ��յ��������______________________��
��3�����в�����ʹ�ⶨ���ƫ�����_______
A����ʼ����ʱƽ�ӣ��յ����ʱ����
B��δ�ñ�Һ��ϴ�ζ���
C�����������ϡ�������ϡ����
��4����ȡ��Ʒw g�����ҷ����������0.01000mol��L-1 I2��ҺVmL����1kg��Ʒ�к�SO2��������____g(�ú�w��V�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Σ����Ϊ���صĴ�����Ⱦ��֮һ,����Ҫ���Ի�ʯȼ�ϵ�ȼ��,�о�CO����ԭSO2����������,��ȼú�糧�����������о�����Ҫ��ֵ��
��.������ѧ�Ƕ��о���Ӧ
(1) C(s)+O2(g)![]() CO2(g) ��H1=-393.5 kJ��mol-1
CO2(g) ��H1=-393.5 kJ��mol-1
CO2(g)+C(s)![]() 2CO(g) ��H2=+172.5 kJ��mol-1
2CO(g) ��H2=+172.5 kJ��mol-1
S(s)+O2(g)![]() SO2(g) ��H3=-296.0 kJ��mol-1
SO2(g) ��H3=-296.0 kJ��mol-1
д��CO ��ԭSO2���Ȼ�ѧ����ʽ:_________________��
(2)����CO��ԭSO2�ķ�Ӧ,����˵����ȷ����______��
A.�ں��º���������,����Ӧ��ϵѹǿ����,��Ӧ�Ѵﵽƽ��״̬
B.ƽ��״̬ʱ,2v��(CO)=v��(SO2)
C.������������,����SO2��Ũ��,CO��ƽ��ת��������
D.�ں��º�ѹ��������,��ﵽƽ��״̬����ϵ�г���N2,SO2��ƽ��ת���ʲ���
��NOx���ŷ���Ҫ����������β��������NO2��NO����������û���̿��NOx����������������Ӧ���£�
��Ӧa��C(s)+2NO(g)![]() N2(g)+CO2(g) ��H=��34.0kJ/mol
N2(g)+CO2(g) ��H=��34.0kJ/mol
��Ӧb��2C(s)+2NO2(g)![]() N2(g)+2CO2(g) ��H=��64.2kJ/mol
N2(g)+2CO2(g) ��H=��64.2kJ/mol
(3)���ڷ�Ӧa����T1��ʱ��������������÷�Ӧ�ڲ�ͬʱ����ϸ����ʵ�Ũ�����£�
ʱ��(min) Ũ��(mol��L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
��0~10min�ڣ�NO��ƽ����Ӧ����v(NO)=___________�������߷�Ӧ�¶ȣ��÷�Ӧ��ƽ�ⳣ��K___________(ѡ����������������С������������)��
��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣻�����ϱ��е������жϸı������������___________(����ĸ)��
A������һ�����Ļ���̿ B��ͨ��һ������NO
C���ʵ���С��������� D��������ʵĴ���
(4)��ijʵ����ģ�ⷴӦb�����ܱ������м���������C��һ������NO2���壬ά���¶�ΪT2�棬��ͼΪ��ͬѹǿ�·�Ӧb������ͬʱ��NO2��ת��������ѹǿ�仯��ʾ��ͼ����Ӷ���ѧ�Ƕȷ�����1050kPaǰ����Ӧb��NO2ת��������ѹǿ����������ԭ��_____________����1100kPaʱ��NO2���������Ϊ___________��

����ij���ʵ�ƽ���ѹ���������ʵ���Ũ��Ҳ���Ա�ʾ��ѧƽ�ⳣ��(����Kp)����T2�桢1.1��106Paʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Kp=___________(�������ʽ��ʾ)����֪�������ѹ(P��)=������ѹ(P��)�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2L���ܱ������У�����1molX��g����2molY��g��������Ӧ��X��g��+m Y��g��![]() 3Z��g����ƽ��ʱ��X��Y��Z����������ֱ�Ϊ30%��60%��10%���ڴ�ƽ����ϵ�м���1molZ��g�����ٴδﵽƽ���X��Y��Z������������䡣������������ȷ����
3Z��g����ƽ��ʱ��X��Y��Z����������ֱ�Ϊ30%��60%��10%���ڴ�ƽ����ϵ�м���1molZ��g�����ٴδﵽƽ���X��Y��Z������������䡣������������ȷ����
A. m=2
B. ����ƽ���ƽ�ⳣ����ͬ
C. X��Y��ƽ��ת����֮��Ϊ1:1
D. �ڶ���ƽ��ʱ��Z��Ũ��Ϊ0.4 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ǻ�ɫ���壬������������Ӱ�������͵�ز��ϵȡ�
ʵ�����Ʊ������������ⶨ����Fe2+��C2O42�����ʵ���֮��ȷ���䴿�ȣ��������£�
��ȡһ�����������������[(NH4)2Fe(SO4)2]���ձ��У�������ˮ��ϡ���ᣬ�����ܽ⣬�ټӱ���H2C2O4��Һ�����ȷ��������ӣ���ȴ�����ˡ�ϴ�ӡ����ɣ��û�ɫ���塣
��ȡm g�����Ƶõľ�������ƿ�У��������ϡ����ʹ���ܽ⣬70��ˮԡ���ȣ���c mol��L1 KMnO4��Һ�ζ����յ㣬����KMnO4��Һv1 mL����������������KMnO4����Ӧ����
�����ζ������Һ�м������п�ۺ�ϡ���ᣬ��У�����Ӧ��ȫ�����ˣ���c mol��L1 KMnO4��Һ�ζ���Һ���յ㣬����KMnO4��Һv2 mL��
�����ظ�����ʵ��3�Σ����㡣
��֪���������������ᡣ
����pH>4ʱ��Fe2+�ױ�O2������
�������������£�KMnO4��Һ�Ļ�ԭ����Ϊ������ɫ��Mn2+��
(1)���м���ϡ�����Ŀ����______��______��
(2)������KMnO4��Һ��Ӧ������______��______��
(3)���м������п�۽���Fe3+��ȫ��ԭΪFe2+����δ��������п�ۣ�������KMnO4��Һ�����V ______v2 mL�����������������������
(4)���У��ζ�ʱ��Ӧ�����ӷ���ʽ��______��
(5)m g�����Ƶõľ����У�Fe2+��C2O42�����ʵ���֮����______���ú�v1�� v2�ļ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����Cu��![]() ��CuO��ɵĻ������ֳ����ݣ�һ�ݻ�����ڼ�����������
��CuO��ɵĻ������ֳ����ݣ�һ�ݻ�����ڼ�����������![]() ��ַ�Ӧ��������ȫ��ת����ͭ��ʱ��������������
��ַ�Ӧ��������ȫ��ת����ͭ��ʱ��������������![]() ������һ�ݻ�����м���
������һ�ݻ�����м���![]() ��Һǡ����ȫ��Ӧ����
��Һǡ����ȫ��Ӧ����![]() ��
��![]() ���費����������ԭ����
���費����������ԭ����![]() ����ЩNO��
����ЩNO��![]() ��״��
��״��![]() ��ϲ�ͨ������ˮ�У�����ȫ������������
��ϲ�ͨ������ˮ�У�����ȫ������������![]() �������������ʵ���Ũ��Ϊ
�������������ʵ���Ũ��Ϊ![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.�����£�pHֵ����14��pHֵ����12������NaOH��Һ�������ͺ�c��H������(10��14��10��10)/2
B.�����£�Ũ��Ϊ1��10��10mol/L��KOH��Һ��pHֵ��ӽ���4
C.��ˮ��ˮϡ�ͣ���Һ�г�ˮ������������ӵ�Ũ�ȶ���С
D.�����£���ͬ�¶���pHֵ����1��������Һ��ˮ�ĵ���̶���pHֵ����13��Ba(OH)2��Һ��ˮ�ĵ���̶����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��[���ʽṹ������]
Cu2O�㷺Ӧ����̫���ܵ��������CuSO4��NaOH�Ϳ���Ѫ��Ϊԭ�ϣ����Ʊ�CuO��
��1��Cu2+��̬��������Ų�ʽΪ____��
��2��![]() �Ŀռ乹��Ϊ____����������������Cu2+��OH��Ӧ������[Cu(OH)4]2��[Cu(OH)4]2�е���λԭ��Ϊ____����Ԫ�ط��ţ���
�Ŀռ乹��Ϊ____����������������Cu2+��OH��Ӧ������[Cu(OH)4]2��[Cu(OH)4]2�е���λԭ��Ϊ____����Ԫ�ط��ţ���
��3������Ѫ��ķ��ӽṹ��ͼ1��ʾ��������̼ԭ�ӵĹ���ӻ�����Ϊ____���Ʋ⿹��Ѫ����ˮ�е��ܽ��ԣ�____������������ˮ������������ˮ������
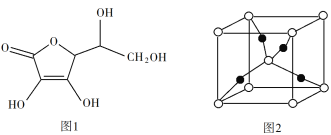
��4��һ��Cu2O��������ͼ2���У�Cuԭ�ӵ���ĿΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������![]() ��˵����ȷ����
��˵����ȷ����
A. �����7��ԭ����ͬһֱ���� B. �����7��̼ԭ����ͬһֱ����
C. ����̼ԭ�ӿ��ܶ���ͬһƽ���� D. �����18��ԭ����ͬһƽ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com