
 £®
£® ·ÖĪö £Ø1£©ŅĄ¾ŻµāŅ×ČÜÓŚĖÄĀČ»ÆĢ¼£¬µāµÄĖÄĀČ»ÆĢ¼ŃÕÉ«ĪŖ×ĻŗģÉ«£¬ĖÄĀČ»ÆĢ¼ĆܶȓóÓŚĖ®µÄĆÜ¶Č½ā“š£»
£Ø2£©ŅĄ¾Ż¹čµ¼µēŠŌ½éÓŚµ¼ĢåÓė¾ųŌµĢåÖ®¼äµÄŠŌÖŹ½ā“š£»
£Ø3£©ŅĄ¾Ż¶ØČŻµÄÕżČ·²Ł×÷½ā“š£»
£Ø4£©Ć÷·ÆĖ®ČÜŅŗÖŠ£¬ĀĮĄė×ÓĖ®½āÉś³ÉµÄĒāŃõ»ÆĀĮ½ŗĢå¾ßÓŠĪüø½ŠŌ£¬Äܹ»Īüø½Ė®ÖŠ¹ĢĢåæÅĮ£ŌÓÖŹ£»
£Ø5£©MgCl2ŹōÓŚĄė×Ó»ÆŗĻĪļ£¬Mg×īĶā²ćĮ½øöµē×Ó±»Į½øöClŌ×ӵƵ½£®
½ā“š ½ā£ŗ£Ø1£©µāŅ×ČÜÓŚĖÄĀČ»ÆĢ¼£¬ĖÄĀČ»ÆĢ¼ĆܶȓóÓŚĖ®µÄĆÜ¶Č£¬ĖłŅŌĖÄĀČ»ÆĢ¼ŻĶČ”µāµÄ±„ŗĶČÜŅŗĻÖĻóĪŖ£ŗ
·Ö²ć£¬ÉĻ²ćŹĒĪŽÉ«ČÜŅŗ£¬ĻĀ²ćĪŖ×ĻÉ«ČÜŅŗ£»
¹Ź“š°øĪŖ£ŗ·Ö²ć£¬ÉĻ²ćŹĒĪŽÉ«ČÜŅŗ£¬ĻĀ²ćĪŖ×ĻÉ«ČÜŅŗ£»
£Ø2£©¹čµ¼µēŠŌ½éÓŚµ¼ĢåÓė¾ųŌµĢåÖ®¼ä£¬ŹĒĮ¼ŗƵİėµ¼Ģå²ÄĮĻ£¬æÉŅŌÓĆĄ“ÖĘŌģ¹āµē³Ų»ņ°ėµ¼Ģå»ņµē×ÓŠ¾Ę¬£»
¹Ź“š°øĪŖ£ŗÖĘŌģ¹āµē³Ų»ņ°ėµ¼Ģå»ņµē×ÓŠ¾Ę¬£»
£Ø3£©¶ØČŻµÄÕżČ·²Ł×÷£ŗĻņČŻĮæĘæÖŠ¼ÓČėÕōĮóĖ®£¬¾ąæĢ¶ČĻß1”«2cmŹ±øÄÓĆ½ŗĶ·µĪ¹Ü£¬¼ĢŠų¼ÓČėÕōĮóĖ®£¬ÖĮČÜŅŗµÄ°¼ŅŗĆęÓėæĢ¶ČĻßĻąĒŠĪŖÖ¹£»
¹Ź“š°øĪŖ£ŗĻņČŻĮæĘæÖŠ¼ÓČėÕōĮóĖ®£¬¾ąæĢ¶ČĻß1”«2cmŹ±øÄÓĆ½ŗĶ·µĪ¹Ü£¬¼ĢŠų¼ÓČėÕōĮóĖ®£¬ÖĮČÜŅŗµÄ°¼ŅŗĆęÓėæĢ¶ČĻßĻąĒŠĪŖÖ¹£»
£Ø4£©Ć÷·ÆĖ®ČÜŅŗÖŠ£¬ĀĮĄė×ÓĖ®½āÉś³ÉµÄĒāŃõ»ÆĀĮ½ŗĢå¾ßÓŠĪüø½ŠŌ£¬Äܹ»Īüø½Ė®ÖŠ¹ĢĢåæÅĮ£ŌÓÖŹ£¬ĖłŅŌĆ÷·Æ¾ßÓŠ¾»Ė®×÷ÓĆ£¬æÉŅŌ×ö¾»Ė®¼Į£»
¹Ź“š°øĪŖ£ŗ¾»Ė®¼Į£»
£Ø5£©MgCl2ŹōÓŚĄė×Ó»ÆŗĻĪļ£¬Mg×īĶā²ćĮ½øöµē×Ó±»Į½øöClŌ×ӵƵ½£¬ÓƵē×ÓŹ½±ķŹ¾ŠĪ³É¹ż³ĢĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ
µćĘĄ ±¾ĢāĪŖ×ŪŗĻĢā£¬æ¼²éĮĖĪļÖŹµÄŠŌÖŹÓėÓĆĶ¾£¬µē×ÓŹ½µÄŹéŠ“£¬Ć÷Č·ŃĪĄąĖ®½ā¹ęĀÉ£¬ĪļÖŹµÄ½į¹¹ÓėŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬×¢ŅāČŻĮæĘæµÄÕżČ·Ź¹ÓĆ·½·ØŗĶ×¢ŅāŹĀĻī£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| XĘųĢå | YČÜŅŗ | Ō¤²āµÄĻÖĻó | 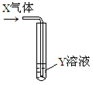 | |
| ¢Ł | CO2 | ±„ŗĶCaCl2ČÜŅŗ | °×É«³ĮµķĪö³ö | |
| ¢Ś | SO2 | Ba£ØNO3£©2ČÜŅŗ | °×É«³ĮµķĪö³ö | |
| ¢Ū | NH3 | AgNO3ČÜŅŗ | °×É«³ĮµķĪö³ö | |
| ¢Ü | NO2 | Na2SČÜŅŗ | °×É«³ĮµķĪö³ö |
| A£® | Ö»ÓŠ¢Ł¢Ś¢Ū | B£® | Ö»ÓŠ¢Ł¢Ś | C£® | Ö»ÓŠ¢Ś | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ś | D£® | ¢Ł¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£®ÅäÖĘ0.10 mol•L-1 NaOHČÜŅŗ | B£®ÖʱøÉŁĮæ°±Ęų |
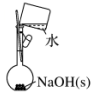 | 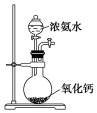 |
| C£®³ĘĮæĒāŃõ»ÆÄĘ¹ĢĢåÖŹĮæ | D£®øÉŌļ°±Ęų |
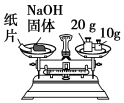 | 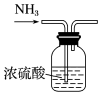 |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com