
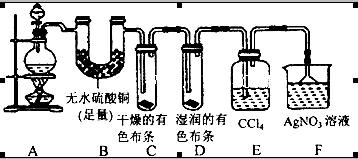
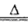 2H2O + Cl2↑+Mn2+;(3分)
2H2O + Cl2↑+Mn2+;(3分)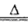 2H2O + Cl2↑+Mn2+;
2H2O + Cl2↑+Mn2+;

科目:高中化学 来源:不详 题型:单选题
| A.二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物 |
| B.将二氧化碳通入硅酸钠溶液可以得到硅酸 |
| C.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强 |
| D.二氧化硅是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质的颜色随核电荷数的增加逐渐加深 |
| B.单质的氧化性随核电荷数的增加而减弱 |
| C.F2通入NaCl水溶液中反应,生成NaF和Cl2 |
| D.可用硝酸酸化的硝酸银溶液来鉴别Cl—、Br— 、I—离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
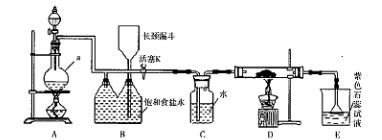
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
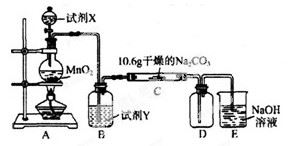
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。 | |
| 步骤2:向A试管中滴加_________: | ①若无明显现象,证明固体中不含碳酸钠; ②若溶液变浑浊,证明固体中含有碳酸钠。 |
| 步骤3:向B试管中滴加________: | 若溶液变浑浊,结合步骤2中的①,则假设一成立:结合步骤2中的②,则假设二成立。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部 | B.②④⑤⑥ | C.②⑤ | D.④⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
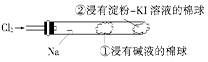
| A.钠在氯气中燃烧产生黄色的火焰 |
| B.反应产生的大量白烟是氯化钠固体 |
| C.棉球①的作用是吸收过量氯气防止产生污染 |
| D.棉球②变蓝色则证明氯气已被碱液完全吸收 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com