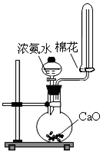
分析:A.利用CaO与H2O剧烈反应,放出大量热,促进NH3.H2O的分解及NH3的挥发逸出;
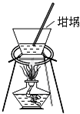
B.在蒸发操作中应用蒸发皿;
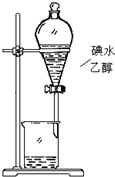
C.乙醇和碘水混溶,不能用分液的方法分离;
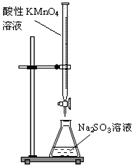
D.酸性高锰酸钾具有腐蚀性,只能用酸式滴定管装液,KMnO4和亚硫酸钠二者发生氧化还原反应.
解答:解:A. CaO与H2O剧烈反应,生成Ca(OH)2,放出大量热,促进NH3.H2O的分解及NH3的挥发逸出,又由于Ca(OH)2是强碱,也促进NH3.H2O的分解及NH3的挥发逸出,反应的化学方程式为:NH3.H2O+CaO═NH3↑+Ca(OH)2,该装置是固体和液体无需加热制取气体的装置符合要求,氨气密度比空气小,用向下排空气法收集正确,故A正确;
B.在蒸发操作中应用蒸发皿,坩埚只能加热固体,不能用来加热液体,故B错误;
C.萃取剂的选择必须符合:溶质在萃取剂中的溶解度比在原溶剂中要大;萃取剂与原溶剂不相溶;萃取剂与溶质不反应,乙醇和水互溶,所以用乙醇无法萃取碘水中的碘,故C错误;
D.酸性高锰酸钾具有腐蚀性,可腐蚀橡胶管,只能用酸式滴定管装液,KMnO4具有强氧化性,亚硫酸钠中+4价的硫具有还原性,二者发生氧化还原反应,可用酸性KMnO4溶液滴定,该装置符合条件,故D正确;
故选AD.
点评:本题主要考查了常见的实验操作,涉及物质的制备、分离和酸碱中和滴定等实验装置或仪器的使用,注意操作的方法和要求,题目难度不大.



 阅读快车系列答案
阅读快车系列答案