
 ��C����������Ӧ�Ļ�ѧ����ʽ
��C����������Ӧ�Ļ�ѧ����ʽ ��
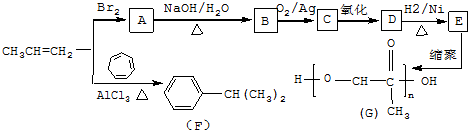
������ ��ϩ���巢���ӳɷ�Ӧ����A��AΪCH3CHBrCH2Br��A����������ˮ��Һ�����������·���ˮ�ⷴӦ����B��BΪCH3CH��OH��CH2OH��B����������C��CΪ ��C��������D��DΪ
��C��������D��DΪ ��D�����������ӳɷ�Ӧ����E��EΪCH3CH��OH��COOH��E����������Ӧ�Ǹ߾���G����ϩ�뱽���Ȼ���������������F
��D�����������ӳɷ�Ӧ����E��EΪCH3CH��OH��COOH��E����������Ӧ�Ǹ߾���G����ϩ�뱽���Ȼ���������������F ������л���Ľṹ�������Լ���ĿҪ��ɽ����⣮
������л���Ľṹ�������Լ���ĿҪ��ɽ����⣮
��� �⣺��ϩ���巢���ӳɷ�Ӧ����A��AΪCH3CHBrCH2Br��A����������ˮ��Һ�����������·���ˮ�ⷴӦ����B��BΪCH3CH��OH��CH2OH��B����������C��CΪ ��C��������D��DΪ
��C��������D��DΪ ��D�����������ӳɷ�Ӧ����E��EΪCH3CH��OH��COOH��E����������Ӧ�Ǹ߾���G����ϩ�뱽���Ȼ���������������F
��D�����������ӳɷ�Ӧ����E��EΪCH3CH��OH��COOH��E����������Ӧ�Ǹ߾���G����ϩ�뱽���Ȼ���������������F ��
��
��1����ϩ�뱽���Ȼ���������������F ��F�ķ���ʽΪC9H12��һ��F�����й�ƽ���̼ԭ��Ϊ�����ϵ�̼�ͼ��ϵ�̼��������7����
��F�ķ���ʽΪC9H12��һ��F�����й�ƽ���̼ԭ��Ϊ�����ϵ�̼�ͼ��ϵ�̼��������7����
�ʴ�Ϊ��C9H12��7��
��2��AΪCH3CHBrCH2Br��A�����й����ŵ���������ԭ�ӣ�A��B�ķ�Ӧ��±�����ļ���ˮ�⣬���Է�Ӧ������ˮ�⣨ȡ������Ӧ��
�ʴ�Ϊ����ԭ�ӣ�ȡ����Ӧ����ˮ�ⷴӦ����
��3��B��C�ķ�ӦΪ���Ĵ���������Ӧ�ķ���ʽΪ ��C����������Ӧ�Ļ�ѧ����ʽΪ
��C����������Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
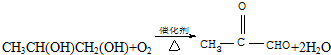
��4��CH3CH��OH��COOH�ж���ͬ���칹�壬����һ���ܷ���������Ӧ��1mol����ͬ���칹���������Ľ����Ʒ�Ӧ����1mol H2��˵����ͬ���칹������к���2��-OH��1��-CHO����Ϊ�����ǻ�����ͬһ̼��ʱ�ṹ���ȶ����������Ϊ  ���ʷ���������ͬ���칹��Ϊ��HOCH2CH��OH��CHO��
���ʷ���������ͬ���칹��Ϊ��HOCH2CH��OH��CHO��
�ʴ�Ϊ��HOCH2CH��OH��CHO��
��5���Ա�ϩ������Ϊԭ�ϣ�NaOH��ҺΪ�������Һ��ȼ�ϵ�أ���ϩ�ǻ�ԭ�����ڸ�������������Ӧ���ڼ�������������̼������ӣ����Ը����ĵ缫��ӦʽΪC3H6+24OH-+18e-=3CO32-+15 H2O��
�ʴ�Ϊ��C3H6+24OH-+18e-=3CO32-+15 H2O��
���� ���⿼���л�����ƶϣ���Ŀ�Ѷ��еȣ���Ϸ�Ӧ������ת���ж���ṹ�ǽ���Ĺؼ�������ij��Ӧ��ϢҪ��ѧ������Ӧ�ã��ܽϺõĿ��鿼�����Ķ�����ѧ������˼ά���������ȵ����ͣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȥһЩ�������� | B�� | ����Fe2+��Ũ�� | ||
| C�� | ������Һ���¶� | D�� | �����¼�ѹ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������NaOH���壬ƽ�������ƶ�����Һ��c��H+������ | |
| B�� | ��ˮ��ƽ�������ƶ���$\frac{c��C{H}_{3}COOH��}{c��C{H}_{3}CO{O}^{-}��}$��С | |
| C�� | ͨ������HCl��ƽ�������ƶ�����Һ��c��H+������ | |
| D�� | ��������CH3COONa���壬ƽ�������ƶ�����Һ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��Na+��+c��H+��=c��OH-��+c��HC2O4-��+c��C2O42-�� | |
| B�� | c��Na+��=2c��HC2O4-��+2c��H2C2O4��+2c��C2O42-�� | |
| C�� | c��OH-��-c��HC2O4-��=c��H+��+2c��H2C2O4�� | |
| D�� | c��Na+����c��C2O42-����c��OH-����c��HC2O4-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �κ�һ��������ԭ��Ӧ���������Ϊԭ��أ�������� | |
| B�� | �����£���pH=2�������pH=12�İ�ˮ�������Ϻ���Һ�ʼ��ԣ�c��NH4+����c��Cl-����c��OH-����c��H+�� | |
| C�� | �κο��淴Ӧ����ƽ�ⳣ��Խ��Ӧ���ʡ���Ӧ���ת����Խ�� | |
| D�� | pH=9��CH3COONa��Һ��pH=9��NH3•H2O��Һ������Һ��ˮ�ĵ���̶���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ��˫��ˮ��ˮ�������Ǵ����� | B�� | ���Ѻ��Ҵ���Ϊͬ���칹�� | ||
| C�� | �Ҵ��������������Ƕ��Ƿǵ���� | D�� | ������Ӳ֬������ͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
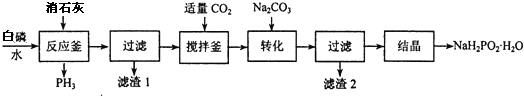
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com