
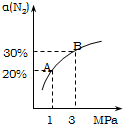
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 将1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ | |
| B. | 平衡状态由A变到B时,平衡常数K(A)<K(B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| D. | 保持压强不变,通入惰性气体,平衡常数不变,平衡不移动 |
分析 A、可逆反应反应物不能完全转化,结合热化学方程式的含义解答;
B、平衡常数只受温度影响,与压强无关;
C、增大压强平衡向体积减小的方向移动;
D、保持压强不变,通入惰性气体,体积变大,平衡常数只受温度的影响.
解答 解:A、热化学方程式N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol表示1mol氮气(g)与3mol氢气(g)反应生成2mol氨气(g),放出的热量为92.4kJ,由于可逆反应反应物不能完全转化,1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量小于92.4kJ,故A错误;
B、平衡常数只受温度影响,与压强无关,增大压强平衡常数不变,故平衡常数K(A)=K(B),故B错误;
C、增大压强平衡向体积减小的方向移动,即向正反应移动,H2的转化率提高,故C正确;
D、保持压强不变,通入惰性气体,体积变大,各组分的分压减小,平衡逆向移动,但是温度不变,所以K不变,故D错误;
故选C.
点评 本题考查化学平衡图象、反应热计算、影响化学平衡与化学反应速率的因素等,难度中等,注意A中热化学方程式的意义.


科目:高中化学 来源: 题型:选择题
| A. | 150mL0.2mol/L氢氧化钠溶液 | B. | 100mL0.3mol/L醋酸溶液 | ||
| C. | 200mL0.2mol/L硫酸溶液 | D. | 150mL0.2mol/L盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 当Al3+恰好完全沉淀时,消耗Ba(OH)2 1.5 mol | |
| B. | 当SO42-恰好完全沉淀时,Al3+全部转化为Al(OH)3 | |
| C. | 当向溶液中加入1.5 mol Ba(OH)2时,反应可用下列离子方程式表示:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 随着加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一般来说,金属越活泼,越易发生腐蚀 | |
| B. | 金属发生腐蚀时表现了明显的氧化性 | |
| C. | 气温越高,金属越易腐蚀 | |
| D. | 金属腐蚀通常分化学腐蚀和电化学腐蚀两类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解池的阳极生成双氧水,阴极生成臭氧 | |
| B. | 电解池中硫酸溶液的pH保持不变 | |
| C. | 产生臭氧的电极反应式为3H2O-6e-=O3+6H+ | |
| D. | 产生双氧水的电极反应式为2H2O-2e-=H2O2+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,过氧化氢
,过氧化氢
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com