

| A. | 非金属性:Y>Z>M | |
| B. | 原子半径:M>Z>Y | |
| C. | Z元素最高价氧化物的水化物的浓溶液具有强氧化性和难挥发性 | |
| D. | 三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
分析 图为元素周期表中短周期的一部分,由元素在周期表的位置可知,X为He,Y为F,Z为S,M为Cl,
A.同周期从左向右非金属性增强,同主族从上到下非金属性减弱;
B.同周期从左到右原子半径逐渐减小;
C.Z为S,对应的最高价氧化物的水化物为硫酸;
D.Y为F,无正价.
解答 解:由元素在短周期的位置可知,Y为F,M为Cl,Z为S,
A.同周期从左向右非金属性增强,同主族从上到下非金属性减弱,则非金属性:Y>M>Z,故A错误;
B.同周期从左到右原子半径逐渐减小,应为Z>M,故B错误;
C.Z为S,对应的最高价氧化物的水化物为硫酸,浓硫酸难挥发,具有强氧化性,故C正确;
D.Y为F,无正价,而M的最高价氧化物对应的水化物酸性最强,故D错误;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意周期律的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. |  用图所示装置可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. |  用图所示装置可降低金属铁的腐蚀速率 | |
| C. |  用图所示装置可测量强酸强碱的中和热 | |
| D. |  用图所示装置可制备Fe(OH)2并能较长时间观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Ca2+>Cl->S2- | B. | 第一电离能:Si>C>N | ||
| C. | 电负性:F>S>Mg | D. | 热稳定性:CH4>H2S>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 变化过程 | 破坏的作用力 |
| A | 干冰升华 | 分子间作用力 |
| B | 钠熔化 | 金属键 |
| C | 氢氧化钠的溶解 | 离子键 |
| D | 水汽化 | 共价键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质的溶液中由水电离出的c(H+)=1×10-10mol/L,则该溶液的pH可能为4或10 | |
| B. | 已知0.1 mol/L NaClO溶液的pH为9.7,0.1 mol/LNaF溶液的pH为7.5,则等体积两溶液中离子总数大小关系为:N(NaClO)>N(NaF) | |
| C. | 将0.2 mol/L的某一元酸HA溶液和0.1 mol/LNaOH溶液等体积混合后溶液pH大于7,则所得溶液中:2c(OH-)=2c(H+)+c(HA)-c(A-) | |
| D. | 向饱和氯水中加入NaOH溶液至pH=7,则所得溶液中:c(Na+)>c(Cl-)>c(C1O-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素原子半径大小为:X>Y>Z>W | |
| B. | 氧化物的水化物的酸性:Z>W | |
| C. | W与Y可形成一种硬度很大的化合物 | |
| D. | W、X、Y三种元素均可以与Z元素形成共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为10的氧原子:${\;}_{10}^{18}$O | B. | 羟基的电子式: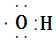 | ||
| C. | Na2S的电子式: | D. | CO2的结构式:O-C-O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应(1)和(2)均为氧化还原反应 | |
| B. | 反应(1)的氧化剂是O2,还原剂是FeO•Cr2O3 | |
| C. | 高温下,O2的氧化性大于Fe2O3小于Na2CrO4 | |
| D. | 生成1mol的Na2Cr2O7时共转移5mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com