
.常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示:
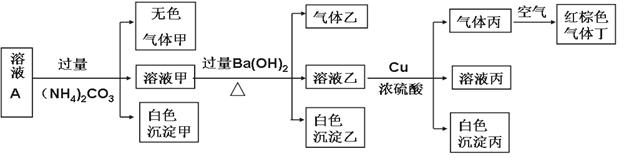
下列有关说法正确的是 ( )
A. 沉淀乙一定有BaCO3,可能有BaSO4
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子
D.生成的甲、乙、丙气体均为无色的易溶于水气体
【知识点】离子反应 B1 D4
【答案解析】C 解析:由溶液pH=1可知溶液为酸性溶液,氢离子浓度为0.1mol/L,溶液中一定不存在与氢离子反应的离子:CO32-;
溶液A中加过量(NH4)2CO3,产生白色沉淀,可以排除Fe2+、Fe3+,原溶液中一定有Al3+;
溶液乙加铜和浓硫酸能产生NO,原溶液中有NO3-,强酸性溶液中有NO3-,则一定没有Fe2+、I-;根据以上分析可知,溶液中存在0.1mol/L的氢离子、0.1mol/L的铝离子,溶液中阳离子带有的电荷为:0.4mol/L;而溶液中除了存在0.1mol/L的硝酸根离子外,还应该含有SO42-离子和Cl-,所以该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子,故C正确;
故答案选C
【思路点拨】本题考查了离子反应,从溶液pH=1,溶液为酸性溶液开始分析,注意当确定了某一种离子存在时,一定要排除与这种离子反应的离子。


科目:高中化学 来源: 题型:
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
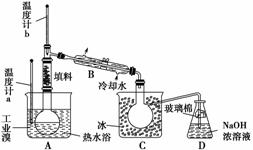
请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下
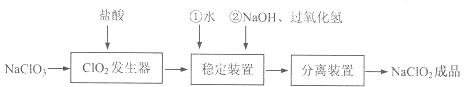
已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一瓶无色溶液,其中可能含有NH4+、K+ 、Mg2+、Ba2+、Al3+ 、Fe3+、I-、Cl-、NO3-、CO32-、SO42-取该溶液进行以下实验:
①该溶液可使pH试纸呈红色;
②取少量溶液加新制氯水及CCl4振荡,可见CCl4层呈现紫色;
③取少量溶液加氯化钡溶液,有白色沉淀生成,加人HNO3后沉淀不溶解;
④取实验③之上层清液,加入硝酸银溶液有白色沉淀生成,加入HNO3后沉淀不溶解;
⑤取少量原溶液加入NaOH溶液呈碱性,在此过程中有白色沉淀生成,而后又逐渐消失,将此溶液加热,有无色气休放出,该气体能使润湿的红色石蕊试纸变蓝。
根据上述实验事实,溶液中肯定存在的离子有_____________________,肯定不存在的离子有_____________________,不能确定是否存在的离子有_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素;少量A与水反应可完全水解而不被氧化或还原,所有反应产物均可溶于水;将A配成水溶液稀释后分成几份,分别加入一系列的试剂,现象如下:
①加入硝酸和硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀生成;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀;
(1)由此判断组成该化合物的元素中,可能存在的卤素有____________,A与水反应后生成的溶液中含有的离子可能有_________________________。
(2)要确定该化合物的分子式,称取11.90g A溶于水稀释至250.0mL,取25.00mL溶液加入足量的高锰酸钾溶液和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重,为2.33g,试确定A的化学式,写出计算过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
某未知溶液可能含Cl-、CO32-、SO32-、Na+、SO42-、Al3+、Fe2+、将少量溶液滴在蓝色石蕊试纸上,试纸变红。另取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成,同时有气体产生,再取上层清液滴加硝酸银溶液,产生白色沉淀,下列判断合理的是
A.一定有Cl- B.一定有SO42-、Fe2+
C.一定没有Al3+、SO32- D.一定没有CO32-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
次氯酸钠(NaClO)和藏氯酸钠(NaClO)都是重要的含氯消毒剂。
(l) NaClO2中,氯元素的化合价为________。
(2)某同学在实验室探究并制作一种家用环保型消毒液(NaClO)发生器,设计了如图的装置,用石墨作电极电解饱和氯化钠溶液。
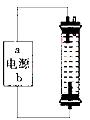
①通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源有b电极名称为_________(填“正”、“负”、“阴”或“阳”)投。
②装置中发生反应的有关化学方程式为________; 充分电解后溶液中各离子浓度由大到小顺序为____________。
③请说出使用该装置生产消毒液的一个优点和一个注意事项____ 。
(3)化学课外活动小组为测定某品牌“84消毒液”中NaClO的含量(单位体积溶液含有 NaCIO的质量),做了如下实验。已知:
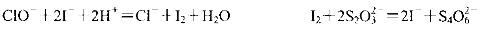
取10 mL该消毒液于锥形瓶中,迅速加入适量的硫酸酸化的碘化钾溶液,密封、充分
混合,暗处放置几分钟。然后加入几滴淀粉溶液,用c mol/L的硫代硫酸钠(Na2S2O3)
标准溶液滴定,平均用去VmL硫代硫酸钠溶液。则该“84消毒液”中NaCIO的含量
为_________g/mL(用含c、V的式子表示)。
(4)以下是过氧化氢法生产亚氯酸钠的工艺流程图:
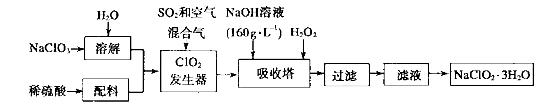
己知:(i)NaClO2 的溶解度随温度升高而增大,适当条件下可结晶析出: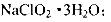
(ii)纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全;
(iii) HClO2可看成是强酸。
①发生器中发生反应的离子方程式为___________________在发生器中鼓入空气的作用可能是__________________。
②吸收塔内的反应的化学方程式为__________________。在吸收塔中为防止被还原成NaCI,所用还原剂的还原性应适中。除外,还可以选择的还原剂_________(填序号)。
A.Na2O2 B.Na2S C.FeCl2
③从滤液中得到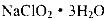 粗晶体的实验操作依次是_________(填序号)。
粗晶体的实验操作依次是_________(填序号)。
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液X中只可能溶有K+、Mg2+、Al3+、AlO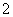 、SiO
、SiO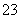 、SO
、SO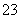 、CO
、CO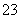 、SO
、SO 中的若干种离子。某同学对该溶液进行了如图实验:
中的若干种离子。某同学对该溶液进行了如图实验:
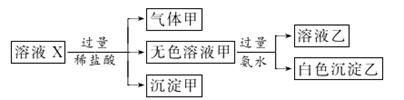
下列判断正确的是( )
A.气体甲一定是纯净物
B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、AlO 和SiO
和SiO 一定存在于溶液X中
一定存在于溶液X中
D.CO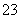 和SO
和SO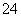 一定不存在于溶液X中
一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
A.C4H10的一种同分异构体只能生成一种氯代物
B.CH3—CH===CH—C≡C—CF3分子结构中6个碳原子可能都在一条直线上
C.某物质的名称为2乙基1丁烯,它的结构简式为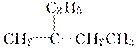
D.制取1,2二溴乙烷的最合理的方法是乙烯与HBr进行加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com