
科目:高中化学 来源: 题型:
| A、在1L 0.1mol/L的NH4NO3溶液中含氮原子数目为0.2NA |
| B、标准状况下22.4 L CH3CH2OH中碳原子数为2NA |
| C、0.2 mol?L-1 NaHCO3溶液中含Na+数为0.2NA |
| D、标准状况下,22.4L Cl2与足量的铁粉完全反应转移电子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| x |
| 2 |
| x |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用量筒量取5.00mL 1.00mol?L-1盐酸于50mL容量瓶中,加水稀释至刻度可配制0.100mol?L-1盐酸 |
| B、用10mL的量筒准确量取9.50mL水 |
| C、向碘水中加入CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| D、稀释浓硫酸时将水倒入浓硫酸中进行搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
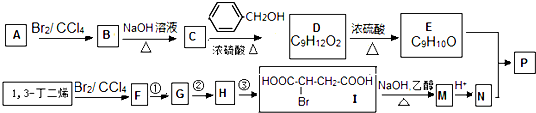
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10.6 g |
| B、5.3 g |
| C、15.9 g |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
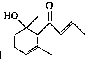 ,可用于制作香水.有关该化合物的下列说法不正确的是( )
,可用于制作香水.有关该化合物的下列说法不正确的是( )| A、分子式为C12H20O2 |
| B、该化合物可使酸性KMnO4溶液褪色 |
| C、1 mol该化合物完全燃烧消耗15.5mol O2 |
| D、1 mol该化合物可与2mol Br2加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com