
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42+以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)第⑤步实验操作需要烧杯、____________、___________等玻璃仪器。
(2)第④步中,相关的离子方程式是: 。
(3)步聚2中,判断沉淀已完全的方法是: 。
(4)除杂试剂Na2CO3、NaOH、BaCl2加入的顺序还可以是
(5)为检验精盐纯度,需配制100 mL 1 mol/L NaCl溶液,右图是该同学转移溶液的示意图,图中的错误是

(6)配制100 mL 1 mol/L NaCl溶液过程中,下列操作情况会使结果偏低的是
A.称量时,托盘天平左盘加砝码,右盘加氯化钠
B.移液前,容量瓶中有少量蒸馏水未倒出
C.定容时,仰视容量瓶刻度线观察液面
D.定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线。
科目:高中化学 来源:2015-2016学年辽宁实验中学分校高一上12月月考化学卷(解析版) 题型:选择题
既能跟盐酸反应,又能跟氢氧化钠溶液反应的氢氧化物是
A.Al2O3 B.MgO C.NaHCO3 D.Al(OH)3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上12月月考化学试卷(解析版) 题型:选择题
甲、乙两烧瓶中各盛有100mL 3mol·L-1的盐酸和氢氧化钾溶液,向两烧瓶中分别加入等质量的铝粉,反应结束测得甲、乙生成的气体体积比为2∶3(相同状况),则加入铝粉的质量为
A.1.60g B.2.70g C. 4.05g D.5.60g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省钦南区高一上学期期中质量调研化学试卷(解析版) 题型:选择题
下列各组混合物中,按照溶解、过滤、蒸发的操作顺序能将它们分离开的是
A.氧化铜和炭粉 B.硝酸钾和氯化钠
C.水和酒精 D.碳酸钠和硫酸钡
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷(解析版) 题型:填空题
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式 。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关.
已知:H2 (g)+Cl2 (g)=2HCl (g)△H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol, E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=
(3)①如图是N2和H2反应生成2mol NH3过程中能量变化示意图,请计算每生成1mol NH3放出热量为: ; ②若起始时向容器内放入1mol N2和3mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为 ;

若在同体积的容器中充入2mol N2和6mol H2,达平衡后放出的热量为Q2 kJ,则Q2 2Q1(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:实验题
利用下图装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.25 mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ/mol):_________ __________________。
(2)倒入NaOH溶液的正确操作是:____________。 (从下列选项中选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1) /℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH =__________ ( 取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)___________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上学期期中(理)化学试卷(解析版) 题型:选择题
下列反应既属于氧化还原反应,又属于吸热反应的是
A.铝片和稀盐酸反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与二氧化碳的反应 D.甲烷在氧气中的燃烧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上学期期中测试化学试卷(解析版) 题型:推断题
下列图示中,A为一种常见的单质,B(白色)、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
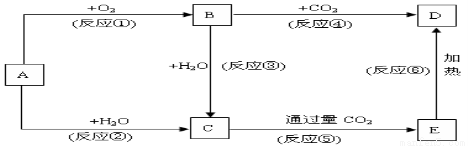
填写下列空白:
(1)写出化学式:A ,B 。
(2)写出反应⑤的离子方程式: 。
(3)写出反应⑥的化学反应方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江大庆实验中学高三上学期期中考试化学试卷(解析版) 题型:填空题
溴、碘及其化合物在工农业生产和日常生活中有重要用途。
Ⅰ.氢溴酸在医药和石化工业上有广泛用途,下图是模拟工业制备氢溴酸的流程:
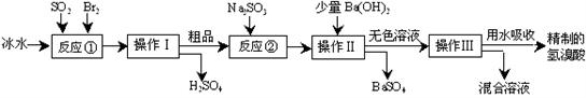
根据上述流程回答下列问题:
(1)反应①中发生反应的离子方程式为 ;使用冰水的目的是
(2)操作Ⅰ的名称是 ;操作Ⅱ的名称是 ;
(3)反应②中加入Na2SO3的目的是 ;但要防止过量,原因是 (用离子方程式表示)
Ⅱ.卤素互化物是指不同卤素原子之间以共价键结合形成的化合物。XX′型卤素互化物与卤素单质结构相似、性质相近, 能与大多数金属反应生成金属卤化物,能与许多非金属单质反应生成相应卤化物,能与水反应等。试回答下列问题:
(4)溴化碘(IBr)与水反应的方程式为IBr +H2O=HBr+HIO下列关于IBr的叙述中不正确的是
A.IBr中溴和碘的化合价均为0价 B.在许多反应中IBr是强氧化剂
C.在IBr与水的反应中,它既是氧化剂又是还原剂 D.与NaOH溶液反应生成NaIO、NaBr和H2O
(5) 在粗碘中含有IBr和ICl,受热时,I2、ICl、IBr均可升华。在粗碘中加入一种物质后,再进行升华,可制得精碘,应加入的物质是
A.H2O B.KI C.Zn D.KCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com