
| A. | 通常状况下,60gSiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数的数值) | |
| B. | 60gSiO2晶体中,含有2NA个Si-O键 | |
| C. | SiO2晶体中与同一硅原子相连的4个氧原子处于同一四面体的4个顶点 | |
| D. | SiO2晶体中含有1个硅原子、2个氧原子 |
分析 A、SiO2晶体是原子晶体,原子晶体是由原子直接构成;
B、根据二氧化硅晶体的结构计算晶体中硅氧键的数目;
C、根据是SiO2晶体立体网状结构的结构特点判断;
D、SiO2晶体中的硅原子和氧原子数取决于晶体的物质的量.
解答 解:A、SiO2晶体是原子晶体,原子晶体是由原子直接构成,晶体中不存在分子,故A错误;
B、在SiO2晶体中,每个硅原子周围有4个硅氧键,所以60gSiO2即1mol二氧化硅晶体中硅氧键的数目为4NA,故B错误;
C、SiO2晶体立体网状结构,每个硅原子周围有4个氧原子,4个氧原子处于同一四面体的4个顶点,故C正确;
D、SiO2晶体中的硅原子和氧原子数取决于晶体的物质的量,故D错误,
故选C.
点评 本题主要考查了SiO2的晶体晶胞的结构,熟记二氧化硅晶胞结构是解题 的关键,难度不大.


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
 合成氨反应是一个放热反应,如图图象中,0-t1是指以N2、H2为初始反应物建立化学平衡的过程,t2-t3指t2时改变某一反应条件(其它条件不变)引起平衡移动的情况,下列叙述正确的是( )
合成氨反应是一个放热反应,如图图象中,0-t1是指以N2、H2为初始反应物建立化学平衡的过程,t2-t3指t2时改变某一反应条件(其它条件不变)引起平衡移动的情况,下列叙述正确的是( )| A. | 改变的条件可能是增大反应体系的压强 | |
| B. | 改变的条件可能是升高温度 | |
| C. | 改变的条件可能是增大了反应器的体积 | |
| D. | t2-t3平衡向逆反应方向移动了 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 置换反应、氧化还原反应、化学反应 | B. | NaOH、电解质、化合物 | ||
| C. | 胶体、溶液、混合物 | D. | Fe2O3、金属氧化物、氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
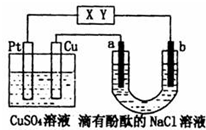
| A. | X极是电源负极,Y极是电源正极 | |
| B. | Pt极上有6.4gCu析出时,b极产生2.24L(标准状况)气体 | |
| C. | a极的电极反应式为:2C1--2e-═C12↑ | |
| D. | 电解过程中 CuSO4溶液的pH逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(X2)=0.15 mol/L | B. | c(Y2)=0.9 mol/L | C. | c(Z2)=0.3 mol/L | D. | c(Q2)=0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/LH2SO4溶液 | |
| B. | 5mL 0.1mol/L Na2S2O3溶液和5mL 0.1mol/LH2SO4溶液 | |
| C. | 5mL 0.1mol/L Na2S2O3溶液和5mL 0.05mol/LH2SO4溶液 | |
| D. | 10mL 0.5mol/L Na2S2O3溶液和10mL 0.05mol/LH2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、H+、S2O32-、PO43- | B. | Pb2+、Hg2+、S2-、SO42- | ||
| C. | Na+、Ba2+、Cl-、OH- | D. | Ca2+、Fe3+、Br-、I- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com