
����Ŀ��[ѡ��5���л���ѧ����]
��1��18-��.
��éȩ�� ![]() ������Ϊ�ϳ������ص��м��壬������éȩ��������ȷ���У� ��
������Ϊ�ϳ������ص��м��壬������éȩ��������ȷ���У� ��
A.����ʽΪC10H18O
B.���ܷ���������Ӧ
C.��ʹ����KMnO4��Һ��ɫ
D.��������7�ֲ�ͬ��ѧ��������
��2��18-��.
���Ѽ����˵��������ͬʱ��R1��O��R2 �� R1��R2����ͨ������Ϊ�����ѡ������ô���ˮ�ij��淽���Ʊ����ѣ����������ั���
R1��OH+ R2��OH ![]() R1��O��R2+ R1��O��R1+ R2��O��R2+H2O
R1��O��R2+ R1��O��R1+ R2��O��R2+H2O
һ����Williamson��Ӧ�Ʊ����ѣ�R1��X+ R2��ONa��R1��O��R2+NaX��ij�����о�С����ϳ� ![]() ���һ��л��ѣ���������������·�߽��жԱȣ�
���һ��л��ѣ���������������·�߽��жԱȣ�
�� ![]()
�� ![]()
�� ![]()
�� ![]()
�ش��������⣺
1��·�ߢ����Ҫ������������
2��A�Ľṹ��ʽΪ��
3��B���Ʊ�������Ӧע��İ�ȫ��������
4����A��B�����һ��л��ѵķ�Ӧ����Ϊ��
5���Ƚ������ϳ�·�ߵ���ȱ�㣺��
6�����״���ͬ���칹���к��б����Ļ����֡�
7��ijͬѧ�ø�Ϊ�����õļױ�������״��ϳ��һ��л��ѣ������·�ߢ�д���ϳ�·����
���𰸡�
��1��C
��2��![]()
![]() ��C2H5��O��C2H5��
��C2H5��O��C2H5��![]()
![]() ��Զ���Դ����ֹ��ը��ȡ����Ӧ��·�ߢ�Ӧ��Խ�Ϊ��ȫ�������ʽϵͣ�·�ߢ���ʽϸߣ��������ױ�ը��������4����
��Զ���Դ����ֹ��ը��ȡ����Ӧ��·�ߢ�Ӧ��Խ�Ϊ��ȫ�������ʽϵͣ�·�ߢ���ʽϸߣ��������ױ�ը��������4���� ![]() +Cl2
+Cl2 ![]()
![]() +HCl����2C2H5OH+2Na��2C2H5ONa+H2������
+HCl����2C2H5OH+2Na��2C2H5ONa+H2������ ![]() +C2H5ONa��
+C2H5ONa�� ![]() +NaCl
+NaCl
��������(1) �⣺A���ɽṹ��ʽ��֪C10H16O����A����
B������ȩ�����ɷ���������Ӧ����B����
C��̼̼˫����ȩ�����ɱ����������������C��ȷ��
D���ṹ���Գƣ���������8�ֲ�ͬ��ѧ�������⣬��D����
��ѡC��(2) �⣺1�������Ϸ�����֪·�ߢ����Ҫ�������� ![]()
![]() ��C2H5��O��C2H5 ��
��C2H5��O��C2H5 ��
���Դ��ǣ�![]()
![]() ��C2H5��O��C2H5��2��AΪ
��C2H5��O��C2H5��2��AΪ ![]()
![]() �� ���Դ��ǣ�
�� ���Դ��ǣ� ![]()
![]() ��3������C2H5ONa��ͬʱ����������ӦԶ���Դ����ֹ��ը�����Դ��ǣ�Զ���Դ����ֹ��ը��4����A��B�����һ��л��ѵķ�Ӧ����Ϊȡ����Ӧ�����Դ��ǣ�ȡ����Ӧ��5��·�ߢ�����϶�ĸ���Ʒ�����ʽϵͣ�����Ϊ��ȫ����·�ߢ���ʽϸߣ��������ױ�ը��������
��3������C2H5ONa��ͬʱ����������ӦԶ���Դ����ֹ��ը�����Դ��ǣ�Զ���Դ����ֹ��ը��4����A��B�����һ��л��ѵķ�Ӧ����Ϊȡ����Ӧ�����Դ��ǣ�ȡ����Ӧ��5��·�ߢ�����϶�ĸ���Ʒ�����ʽϵͣ�����Ϊ��ȫ����·�ߢ���ʽϸߣ��������ױ�ը��������
���Դ��ǣ�·�ߢ�Ӧ��Խ�Ϊ��ȫ�������ʽϵͣ�·�ߢ���ʽϸߣ��������ױ�ը��������6�����״���ͬ���칹�壬�纬��2��ȡ��������Ϊ�����ӣ����������ڼ�����֣��纬��1��ȡ��������Ϊ�����ѣ�����4�֣����Դ��ǣ�4��7���ױ�������״��ϳ��һ��л��ѣ������ȷ����� ![]() +Cl2
+Cl2 ![]()
![]() +HCl���ڷ���2C2H5OH+2Na��2C2H5ONa+H2����Ȼ������
+HCl���ڷ���2C2H5OH+2Na��2C2H5ONa+H2����Ȼ������ ![]() +C2H5ONa��
+C2H5ONa�� ![]() +NaCl��
+NaCl��
���Դ��ǣ��� ![]() +Cl2
+Cl2 ![]()
![]() +HCl����2C2H5OH+2Na��2C2H5ONa+H2������
+HCl����2C2H5OH+2Na��2C2H5ONa+H2������ ![]() +C2H5ONa��
+C2H5ONa�� ![]() +NaCl��
+NaCl��
�����㾫����������Ĺؼ����������л���Ľṹ�����ʵ����֪ʶ�������л���������ص㣺������ˮ�����������͡��ƾ��������л��ܼ�����Ϊ�ǵ���ʣ������磻�����۷е�ϵͣ�������ȼ�գ��ֽ⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���3mol A��1mol B�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A��g��+B��g��xC��g��+2D��g����2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8mol D�������C��Ũ��Ϊ0.2molL��1 �� �����ж���ȷ���ǣ� ��
A.A��ת����Ϊ40%
B.2 min��B�ķ�Ӧ���� Ϊ0.2 mol��Lmin����1
C.x=2
D.�����������ܶȲ��䣬������÷�Ӧ�Ѵﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����ܵ���ĵ�����ǣ�������
A. �������Һ B. ����ʯ��ˮ C. �ƾ� D. �Ȼ��ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʷ�����ȷ���ǣ�������
�ٻ������ᡢ��ˮ��ˮ������ˮ��
�ڻ����CaCl2���ռ�۱���ϩ��O3
�۵���ʣ�H2SO4�������������ᡢ���ᱵ
��ͬ�������壺C60��C70�����ʯ��ʯī
A. �٢� B. �ڢ� C. �ڢ� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2��g��+O2��g��2SO3��g�����Ʊ��������Ҫ��Ӧ������������ȷ���ǣ� ��
A.����V2O3���ı�÷�Ӧ���淴Ӧ����
B.����Ӧ��ϵ��ѹǿ����Ӧ����һ������
C.�÷�Ӧ�Ƿ��ȷ�Ӧ�������¶Ƚ����̷�Ӧ�ﵽƽ���ʱ��
D.��t1��t2ʱ�̣�SO3��g����Ũ�ȷֱ���c1��c2 �� ��ʱ����t1��t2�ڣ�SO3��g�����ɵ�ƽ������Ϊv= ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[ѡ��3�����ʽṹ������]
��1��19-�� ����������ȷ���У� ��
A.ijԪ��ԭ�Ӻ�����������������ѧ@������������5���������������Ϊ+7
B.��Ԫ�صĵ�һ���ڶ������ֱܷ�С��þԪ�صĵ�һ���ڶ�������
C.������������������Ծ����ڴ���������Ժ�������
D.���ǻ�����ȩ���۵���ڶ��ǻ�����ȩ���۵�
��2��19-�� ��A��Ԫ�ؼ��仯�����ڲ��ϵȷ�������Ҫ��;���ش��������⣺
1��̼��һ�ֵ��ʵĽṹ��ͼ��a����ʾ���õ��ʵľ�������Ϊ �� ԭ�Ӽ���ڵĹ��ۼ������� �� ̼ԭ�ӵ��ӻ��������Ϊ��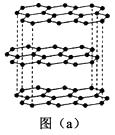

2��SiCl4���ӵ�����ԭ�ӵļ۲���Ӷ���Ϊ �� ���ӵ����幹��Ϊ �� �������ӣ�����ԡ��Ǽ��ԡ�����
3����±����SiX4�ķе�Ͷ�±��ǦPbX2���۵���ͼ��b����ʾ��
��SiX4�ķе���F��Cl��Br��I�������ߵ�ԭ������
�ڽ��SiX4�ķе��PbX2���۵�ı仯���ɣ����ƶϣ���F��Cl��Br��I����PbX2�еĻ�ѧ�������������������������ǿ�������䡱��������
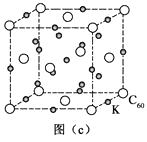
4��̼����һ�ֵ���C60��������γɵ��³������������ṹ��ͼ��c����ʾ��Kλ������������Ϻ���������ڲ����˻�����Ļ�ѧʽΪ���侧������Ϊ1.4 nm�������ܶ�Ϊ
g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ʊ������������һ����Ҫ���ʣ����������������;�㷺����ͼ��ʾ���������̵���Ӧ��ƽ�ⳣ������ֵ��IgK�����¶ȵĹ�ϵ��
��N2+3H22N2H3 ��N2+3O22NO
����ͼ�е������ж�����˵����ȷ���ǣ� ��
A.��Ӧ�ٺ͢ھ�Ϊ���ȷ�Ӧ
B.�����¶ȣ���Ӧ�ٵķ�Ӧ���ʼ�С
C.�ڳ����£����÷�Ӧ�ٹ̵������÷�Ӧ�ڹ̵���Ӧ�̶����ܴ�
D.��1000��ʱ����Ӧ�ٺͷ�Ӧ����ϵ��N2��Ũ��һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʳƷ�м���ɷֲ���Ӫ��ǿ�������ǣ� ��
A.ʳ�μӵ�
B.�������
C.ʳƷ�м���
D.�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2015���Ϻ����ֲ�����ҩ��³����E���ṹ��ʽΪ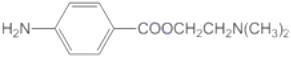 ���������ϳ�·������ͼ��ʾ�����ַ�Ӧ�Լ���������ʡ�ԣ���
���������ϳ�·������ͼ��ʾ�����ַ�Ӧ�Լ���������ʡ�ԣ���
��1����A��һ��̼ԭ�ӣ���һ�����ֻ��3�ֵ�A��ͬϵ��������� ��
��2��д����Ӧ�Լ��ͷ�Ӧ��������Ӧ�� ����
��3����Ʒ�Ӧ�ڵ�Ŀ���� ��
��4��B�Ľṹ��ʽΪ ��C�������� ��
��5��д��һ����������������D��ͬ���칹��Ľṹ��ʽ��
�ٷ����廯���� ���ܷ���ˮ�ⷴӦ ����3�ֲ�ͬ��ѧ��������ԭ��
1 mol��������NaOH��Һ����������� mol NaOH��
��6����³����������ϳ�·���У���һ���ϳ�·����ڶ�������������Ȳ�̫���룬������ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com