
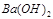 的稀溶液中
的稀溶液中 已知
已知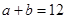 向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示
向该溶液中逐滴加入PH=c的盐液,测得混合溶液的部分PH如下表所示| | 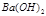 溶液体积/ml 溶液体积/ml | 盐液的体积/ml | 溶液的PH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
科目:高中化学 来源:不详 题型:单选题
A.2H+(aq)+SO42-(aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(1)△H=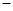 57.3 kJ/mol 57.3 kJ/mol |
B.KOH(aq)+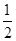 H2 SO4(aq)= H2 SO4(aq)=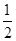 K2SO4(aq)+H2O(l)△H= K2SO4(aq)+H2O(l)△H=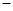 57.3kJ/mol 57.3kJ/mol |
C.C8H18(I)+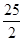 O2(g)=8CO2(g)+9H2O△H= O2(g)=8CO2(g)+9H2O△H=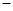 5518 kJ/mol 5518 kJ/mol |
D.2C8H18(g)+25O2(g)=16CO2(g)+18H2O(1)△H=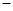 5518 kJ/mol 5518 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
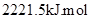 -1,下列有关说法正确的是( )
-1,下列有关说法正确的是( )| A.奥运火炬燃烧主要是将化学能转变为热能和光能 |
| B.丙烷的沸点比正丁烷高 |
| C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极 |
| D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH4+)+ c(H+) =c(OH-) |
| B.c(Na+)=c(Cl-)>c(H+)=c(OH-) |
| C.c(NH4+)+c(NH3·H2O) =2c(Cl-) |
| D.c(NH4+) >c(NH3·H2O)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HF与CaCl2反应产生沉淀 |
| B.25℃时0.2mol·L-1HF溶液中pH=2 |
| C.Ksp(CaF2)随温度和浓度的变化而变化 |
| D.该体系中最终没有氟化氢分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.0 | B.4.2 | C.4.0 | D.3.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10 | B.50 | C.5×103 | D.104 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com