
【题目】下列有关图像说法不正确的是

A. 图①:向等浓度的碘化钠和氯化钠的混合溶液中加入硝酸银溶液
B. 图②:向pH和体积均相同的盐酸和醋酸两种溶液中分别加水稀释
C. 图③:向饱和Ca(OH)2溶液中通入CO2
D. 图④:向Ba(OH)2溶液中加入稀H2SO4
【答案】C
【解析】A. 图①:向等浓度的碘化钠和氯化钠的混合溶液中加入硝酸银溶液,碘化银与氯化银比,溶度积小而相对分子质量大,故先产生碘化银沉淀质量增大多,后产生氯化银质量增加小,选项A正确;B、醋酸为弱酸存在电离平衡,随着水的加入电离平衡正向移动,氢离子浓度降低慢,选项B正确;C、向饱和Ca(OH)2溶液中通入CO2先生成碳酸钙沉淀,后沉淀溶解,但产生沉淀和沉淀溶解所消耗的二氧化碳的量相等,选项C不正确;D、向Ba(OH)2溶液中加入稀H2SO4,开始时产生硫酸钡和水,溶液中离子浓度大量减少,导电能力减弱直至为0,当硫酸过量后,离子浓度增大,导电能力增强,选项D正确。答案选C。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是
A. 标准状况下,11.2L14CO2含有的中子数为11NA
B. 5.6gFe粉与足量S粉加热充分反应转移的电子数为0.2NA,
C. 1molNa2O2固体中所含离子数目为4NA
D. 1LpH=6的纯水中含有OHˉ的数目为10-8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来。
B. 聚合物![]() 可由单体CH3CH=CH2和CH2=CH2加聚制得。
可由单体CH3CH=CH2和CH2=CH2加聚制得。
C. 相对分子质量为72的某烷烃,一氯代物有4种。
D. 植物油氢化、塑料和橡胶的老化过程中均发生了加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000 mol/L盐酸滴入20.00 mL 1.000 mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法正确的是

A. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
B. a点由水电离出的c(H+)=1.0![]() mol/L
mol/L
C. b点:c(NH![]() )+c(NH3·H2O)=c(Cl-)
)+c(NH3·H2O)=c(Cl-)
D. c点:c(Cl-)=c(NH![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下:CO(g)+H2O(g)![]() CO2(g)+H2(g),在两个均为2L的密闭容器中以不同的氢碳比[n(H2O)/n(CO)]充入H2O(g)和CO,CO的平衡转化率α(CO)与温度的关系如下图所示。
CO2(g)+H2(g),在两个均为2L的密闭容器中以不同的氢碳比[n(H2O)/n(CO)]充入H2O(g)和CO,CO的平衡转化率α(CO)与温度的关系如下图所示。

①R点平衡常数K=__________________。
②氢碳比X_________2.0(填“>”或“<”或“=”),判断的理由是______________。
③下列能提高CO平衡转化率的措施有_________。
A.使用高效催化剂 B.通入He气体使体系的压强增大
C.降低反应温度 D.投料比不变,增加反应物的浓度
(2)已知:反应I:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0
4NO(g)+6H2O(g) △H<0
反应II:4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H<0
2N2(g)+6H2O(g) △H<0
氨催化氧化时会发生上述两个竞争反应I和Ⅱ。为分析该催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,反应关系如图,该催化剂在高温时选择反应_________(填“I”或“II”)。520℃时,4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g)的平衡常数K=_______(只需列出数字计算式)。
2N2(g)+6H2O(g)的平衡常数K=_______(只需列出数字计算式)。

(3)以连二硫酸根(S2O42-)为介质,使用间接电化学法可处理燃煤烟气中的NO,装置如图所示:

①阴极区的电极反应式为___________。
②NO吸收转化后的主要产物为NH4+,若通电时电路中转移了0.3mol e-,则此通电过程中理论上吸收的NO在标准状况下的体积为___________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铁离子(Fe3+)最外层电子排布式为______,其核外共有______种不同运动状态的电子。
(2)硒、砷、溴三种元素的第一电离能从大到小的顺序为___________(用元素符号表示)。
(3)两种三角锥形气态氢化物PH3和NH3的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因_____________________________________________________________。
(4)常温下PCl5是白色晶体,在148℃时熔化成能导电的熔体。该熔体由A、B两种微粒构成,A、B分别与CCl4、SF6互为等电子体,则A的化学式为__________________,其中心原子杂化方式为_______________。
(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为ρg·cm-3),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。


①与Au距离最近的Cu个数为________。
②该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为__________,则晶胞中Cu原子与Au原子中心的最短距离d=________cm。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为__________(![]() )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到1mol/L盐酸中,待合金完全溶解后(盐酸有剩余),再往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化如图所示。下列说法中错误的是( )
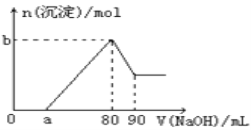
A. 盐酸的体积为80mL
B. a的取值范围为0<a<50
C. 当a值为30时,b值为0.01
D. n(Mg2+)<0.025mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含BeO:25%、CuS:71%、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:

已知:I.铍、铝元素化学性质相似
II.常温下:Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=-2.1×10-13
(1)滤液A的主要成分除NaOH外,还有_____ (填化学式),写出反应I中含铍化合物与过量盐酸反应的离子方程式_____________。
(2)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择最合理步骤顺序______。
a.加入过量的NaOH b.通入过量的CO2 c.加入过量的氨水
d.加入适量的HC1 e.过滤 f.洗涤
②从BeCl2溶液中得到BeCl2固体的操作是________________。
(3)①MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应II中CuS 发生反应的化学方程式______________。
②若用浓HNO3溶解金属硫化物,缺点是____________(任写一条)。
(4)溶液D中含c(Cu2+)=2.2mol/L、c(Fe3+)=0.008mol/L c(Mn2+)=0.01mol/L,逐滴加入稀氨水调节pH可依次分离,首先沉淀的是___ (填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH值大于____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋硝香豆素是一种治疗心脑血管疾病的药物,能阻碍血栓扩展。醋硝香豆素可以通过以下方法合成(部分反应条件省略)。

已知:a.![]()
b.丙二酸酐为一分子丙二酸脱去两分子水后的产物,其分子式为C3O2,该分子为链状结构
回答以下问题:
(1)醋硝香豆素中含有官能团的名称是___________________。
(2)C的结构简式为:_____________。
(3)E与G生成醋硝香豆素的反应类型为____________。
(4)写出题中苯酚与丙二酸酐生成G的化学方程式_______________________。
(5)反应③的化学方程式为_______________________________________。
(6)关于E物质,下列说法正确的是_______(填字母序号)。
a.在核磁共振氢谱中有五组吸收峰
b.可以用银镜反应鉴别D和E
c.可以发生加成反应、缩聚反应、氧化反应和还原反应
d.存在顺反异构
(7)分子结构中只含有一个环,且同时符合下列条件的G的同分异构体共有____种。
①可与氯化铁溶液发生显色反应;②可与碳酸氢钠溶液反应生成二氧化碳气体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com