
【题目】将下列液体分别与溴水混合并振荡,静置后溶液分为两层,下层几乎无色的是
A. 酒精 B. 苯 C. CCl4 D. 氢氧化钠溶液
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为有机物,其中A常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如图转化关系。已知醛基在氧气中易被氧化成羧基,请回答下列问题:

(1)A的官能团名称为__________。
(2)属于取代反应的有______________(填对应编号)。
(3)满足下列条件的有机物有_________种。
a.与B互为同系物 b.含有5个碳原子
(4)写出下列编号对应反应的化学方程式:
②________________________________________________________。
④_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.2017年08月08日21时19分46秒在四川阿坝州九寨沟县发生7级地震。地震后,为防止疫病流行,全国各地向灾区运送了大量的消毒剂、漂白剂等。请回答下列相关问题:
(1)次氯酸盐是一些漂白剂和消毒剂的有效成分。84消毒液的有效成分是次氯酸钠,制取该消毒液的化学方程式为_______。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在一定条件下与SO2反应制得。该反应的离子方程式为:_______。
(3)漂白剂亚氯酸钠(NaClO2)在常温黑暗处可保存一年,但亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。
当1 molHClO2发生分解反应时,转移电子的物质的量是_________mo1。
Ⅱ.溴及其化合物广泛应用在有机合成、化学分析等领域。
(4)海水提溴过程中溴元素的变化如下:
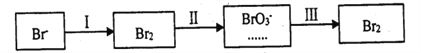
①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。调海水PH可提高Cl2的利用率.用平衡原理解释其原因是______________。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列方程式。
_____Br2+_______Na2CO3 =______NaBrO3+_____CO2+____。
(5)NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
粒子 | I2 | Br2 | IO3- |
物质的量/mol | 0.5 | 1.3 |
则原溶液中NaI的物质的量是_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(A)=3v(B),v(C)=2v(B),则此反应可表示为( )
A. 3A+2B=4C B. 2A+3B=6C C. 3A+2B=C D. 2A+3B=4C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)原子序数为24的元素原子中有___________个电子层,___________个能级,_________个未成对电子,位于元素周期表的___________区。
(2)在下列物质中:①N2、②H2O、③NaOH、④MgCl2、⑤C2H4、⑥Na2O2(用序号填空)
其中只含有非极性键的是___________;只含有极性键的是___________;只含有离子键的是___________;既含有非极性键又含有极性键的是___________;含有非极性键的离子化合物是___________。
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的___________键更稳定(填“σ”或“π”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KAl(SO4) 2 ·12H2O]易溶于水,不易溶于乙醇,在生产、生活中有广泛用途。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量的SiO2、FeO·xFe2O3)制备明矾的工艺流程如下:

回答下列问题:
(1)酸浸时为提高铝的浸取率,可采取的措施是_________(填标号)。
a.改用同浓度的硝酸 b.用硫酸多次浸取
c.浸取时间缩短一半 d.适当升高温度
(2)滤渣1的成分是__________;滤渣2经过处理可以制得一种高效的无机高分子混凝剂,其化学式为[Fe2(OH)n(SO4)(3-0.5n)]m,则该物质中铁元素的化合价为___________。
(3)检验滤液A中含有Fe2+的实验方案及现象是________________________________________。
(4)已知常温下Ksp[Fe(OH)3]=4.0×10-38,当调节溶液的pH=3时,溶液中c(Fe3+)=____________。
(5)操作Ⅱ中包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,使用酒精洗涤明矾晶体的目的是___________________________________________________________________;明矾净水的原理是_______________________________________(写离子方程式)。
(6)已知在pH=3和加热条件下,MnO4-可与Mn2+反应生成MnO2,则上述流程图中加入适量MnSO4发生反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的俗称和分类都正确的是
A. CuSO45H2O(胆矾、混合物) B. Cu2(OH)2CO3(铜绿、盐)
C. Na2CO3(纯碱、碱) D. Ca(OH)2(生石灰、碱)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是
A. ①②③④ B. ②③ C. ①②④ D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com