
【题目】盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式: 。
【答案】
CO(g)+FeO(s)=Fe(s)+CO2(g) △H=-218.0kJ/mol
【解析】
试题分析:①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol,②3Fe2O3(s)+CO(g) ═2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol,③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ/mol,依据盖斯定律计算,(①×3-③×2+②)×![]() ,得到CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式为:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=-218.0kJ/mol;故答案为:CO(g)+FeO(s) ═Fe(s)+CO2(g) △H=-218.0kJ/mol。
,得到CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式为:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=-218.0kJ/mol;故答案为:CO(g)+FeO(s) ═Fe(s)+CO2(g) △H=-218.0kJ/mol。


科目:高中化学 来源: 题型:
【题目】在一定条件下,容积为2 L的密闭容器中,将2 mol L气体和3 mol M气体混合,发生如下反应:2L(g)+3M(g)![]() xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
xQ(g)+3R(g),10s末,生成2.4 mol R,并测得Q的浓度为0.4 mol·L-1。计算:
(1)10 s末L的物质的量浓度为_____________。
(2)前10 s内用M表示的化学反应速率为_____________。
(3)化学方程式中x值为_____________。
(4)在恒温恒容条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
(5)在恒温恒压条件,往容器中加入1 mol氦气,反应速率________(增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应①X(g)+2Y(g)![]() 2Z(g)、②2M(g)
2Z(g)、②2M(g)![]() N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
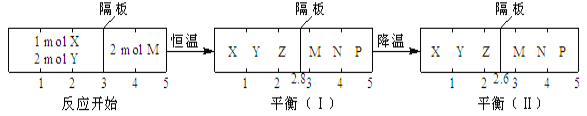
下列判断正确的是( )
A. 反应①的正反应是吸热反应
B. 达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C. 达平衡(I)时,X的转化率为5/11
D. 在平衡(I)和平衡(II)中,M在隔板右边气体中的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气(主要成分CO2、CO、SO2、NOX) 的排放对环境有很大的影响。
I.利用氨水作吸收液是当前有效捕捉CO2的方法,经过可逆反应生成NH4HCO3。生成的NH4HCO3分解可得到CO2,从而实现吸收液的再生。
(1)写出氨水捕捉CO2 的化学方程式 。
(2)已知:NH4HCO3 溶液显碱性,下列说法不正确的是 。
a.c(NH3·H2O)>c(H2CO3)
b.c(NH4+)>c(HCO3—)>c(OH—)>c(H+)
c.c(NH3·H2O)+c(NH4+)=c(H2CO3)+c(HCO3—)
d.c(HCO3—)+2c(CO32—)+c(OH—)=c(H+)+c(NH4+)
(3)如图是氨水吸收CO2 的脱除率随温度变化的关系图。
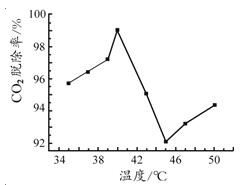
应用平衡移动原理分析 CO2 在 40℃-45℃ 脱除率降低可能的原因 。
II.SO2、NOX 可以经 O3 预处理后用 CaSO3 水悬浮液吸收,可减少烟气中SO2、NOX 的含量。O3 氧化烟气中 NOX 的主要反应的热化学方程式为:
(4)用CaSO3水悬浮液吸收烟气中NO2时,清液 ( pH约为8) 中SO32-将NO2转化为NO2-,其离子方程式为 。
(5)CaSO3水悬浮液中加入Na2SO4溶液能提高NO2 的吸收速率,用平衡移动原理解释其主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,离子方程式正确的是
A. CO32— + Ba2+ → BaCO3↓
B. HCO3— + OH— → H2O + CO32—
C. HCO3— + Ba2+ + OH— → H2O + BaCO3↓
D. 2HCO3— + Ba2+ + 2OH— → BaCO3↓+ 2H2O + CO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是
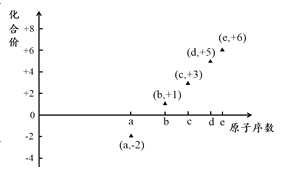
A. 31d和33d属于同种核素
B. 气态氢化物的稳定性:a>d>e
C. 工业上常用电解法制备单质b和c
D. a和b形成的化合物不可能含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于微量元素的一组是( )
A. Cl、Fe、S、N、Cu B. B、Cl、Zn、Mn、Mo
C. C、H、N、P、Mn D. N、P、K、B、Fe、I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。
(1)高湿条件下,写出大气中SO2转化为HSO3—的方程式: 。
(3)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如下:
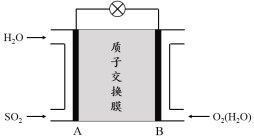
① 质子的流动方向为 (“从A到B”或“从B到A”)。
② 负极的电极反应式为 。
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。SO2烟气脱除的一种工业流程如下:
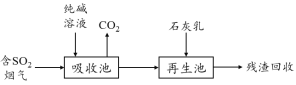
① 用纯碱溶液吸收SO2将其转化为HSO3—,反应的离子方程式是 。
② 若石灰乳过量,将其产物再排回吸收池,其中可用于吸收SO2的物质的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
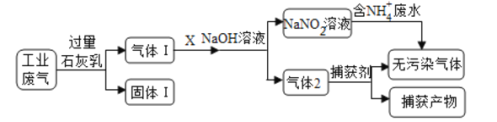
下列说法不正确的是( )
A.固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B.X可以是空气,且需过量
C.捕获剂所捕获的气体主要是CO
D.处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-=N2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com