
| A. | 4.48 L | B. | 5.6 L | C. | 6.7 L | D. | 7.8 L |
分析 Ag+和Cl-反应生成AgCl沉淀,电解时溶液中不存在Ag+,阴离子放电顺序为Cl->OH-,若在一极析出0.3molCu,阴极得到电子为0.3mol×2=0.6mol,结合两极转移电子数目相等以及电极方程式计算.
解答 解:Ag+和Cl-反应生成AgCl沉淀,电解时溶液中不存在Ag+,
反应后溶液中存在0.4molCu2+、0.4molCl-,
若在一极析出0.3molCu,阴极得到电子为0.3mol×2=0.6mol,
阳极首先发生:2Cl--2e-=Cl2↑,然后发生4OH--4e-=O2+2H2O,
则0.4molCl-生成0.2molCl2,失去0.4mol电子,在反应中4OH--4e-=O2+2H2O,转移0.2mol电子,生成0.05molO2,
则气体的体积为(0.2mol+0.05mol)×22.4L/mol=5.6L,
故选B.
点评 本题考查电解原理,为高考常见题型,侧重于学生的分析能力的考查,注意把握离子的放电顺序,为解答该题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1molCl2作为反应物,转移电子数一定为2NA | |
| B. | 25℃时,1.0LpH=13的Ba(OH)2溶液中水电离的OH-数目为0.1NA | |
| C. | 17g烃基和17gOH-含有的电子数均为10NA | |
| D. | 标准状况下,NA个NO分子和0.5NA个O2分子充分反应后气体分子数小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=2b时,生成沉淀98.5ag | |
| B. | a≤b≤2a时,溶液中含n(NaOH):n(Na2CO3)=(2a-b):(b-a) | |
| C. | 0<b<2a时,沉淀质量随着NaHCO3的加入而不断增加 | |
| D. | b=$\frac{3}{2}$a时,总离子方程式为:3HCO3-+2Ba2++3OH-=2BaCO3↓+CO32-+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
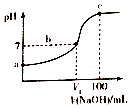 已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )
已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )| A. | a点溶液的pH=4 | |
| B. | b点溶液中存在:c(A-)>c(Na+)>c(H+)=c(OH-) | |
| C. | b点c(HA)/c(A-)=5 | |
| D. | c点c(A-)+c(H+)=c(Na+)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②⑤ | B. | 只有①②③⑤ | C. | 只有②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将浓硝酸加入盛有铂、金的烧杯中,不反应,再加入一定量浓盐酸后,铂、金溶解,不能说明浓硝酸氧化性比浓盐酸强 | |
| B. | 石英玻璃、普通玻璃、陶瓷及水泥均属于硅酸盐产品 | |
| C. | 电解AlCl3水溶液,阴极周围出现白色胶状沉淀,说明Al(OH)3胶体粒子带正电荷 | |
| D. | 气体甲通入溶液乙,溶液乙的颜色褪去,说明气体甲具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:X<W<Z | |
| B. | W、X、Y元素形成的盐溶于水,溶液一定呈中性 | |
| C. | W与X形成的常见化合物中阴、阳离子个数比均为1:2 | |
| D. | 1 mol Z 的单质与足量的NaOH溶液反应转移电子数1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.125mol•L-1•min-1 | B. | 0.100 mol•L-1•s-1 | ||
| C. | 0.200 mol•L-1•min-1 | D. | 0.375 mol•L-1•s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com