
����Ŀ��(1)˳-1��2-����������ͷ�-1��2-����������ɷ�������ת����

�÷�Ӧ�����ʷ��̿ɱ�ʾΪ��v(��)=k(��)c(˳)��v(��)=k(��)c(��)��k(��)��k(��)��һ���¶�ʱΪ�������ֱ���������淴Ӧ���ʳ������ش��������⣺
��֪��t1�¶��£�k(��)=0.006s��1��k(��)=0.002s��1�����¶��·�Ӧ��ƽ��ʱ��c(��-1��2-����������)��c(˳-1��2-����������)=_____________��
�÷�Ӧ�Ļ��Ea(��)С��Ea(��)����![]() ________0(����С����������������������)��
________0(��������������������������)��
(2)����ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ���������Ӧ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�
CO2(g)+3 H2(g) CH3OH(g)+H2O(g)��H1=-53.7kJ��mol-1 I
CO2(g)+ H2(g) CO(g)+H2O(g)��H2 II
ijʵ���ҿ���CO2��H2��ʼͶ�ϱ�Ϊ1:2.2��������ͬ��Ӧʱ��������ʵ�����ݣ�
T��K�� | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
����ע��Cat.1:Cu/ZnO���װ���Cat.2:Cu/ZnO����Ƭ���״�ѡ���ԣ�ת����CO2�����ɼ�ȩ�İٷֱȣ�
��֪����CO��H2��ȼ���ȷֱ�Ϊ-283.0kJ��mol-1��-285.8kJ��mol-1
��H2O(l)=H2O(g) ��H3=44.0kJ��mol-1
��ش�(�������¶ȶ���H��Ӱ��)����ӦII����H2= kJ��mol-1��
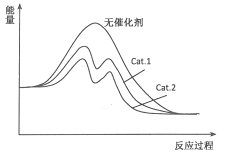
����ͼ�зֱ�I����������Cat.1����Cat.2�������������Ӧ����-������ʾ��ͼ(��ͼ�б�ע����Ӧ������)��

���𰸡�
(1)3����(2)+41.2��
 ��
��
��������
���������(1)����v(��)=k(��)c(˳)��k(��)=0.006s-1����v(��)=0.006c(˳)��v(��)=k(��)c(��)��k(��)=0.002s-1����v(��)=0.002c(��)����ѧƽ��״̬ʱ���淴Ӧ������ȣ���0.006c(˳)=0.002c(��)�����¶��·�Ӧ��ƽ�ⳣ��ֵK1=![]() =
=![]() =3���÷�Ӧ�Ļ��Ea(��)С��Ea(��)��˵���ϼ����յ�����С�ڳɼ��ͷŵ����������÷�ӦΪ���ȷ�Ӧ������HС��0���ʴ�Ϊ��3��С�ڣ�
=3���÷�Ӧ�Ļ��Ea(��)С��Ea(��)��˵���ϼ����յ�����С�ڳɼ��ͷŵ����������÷�ӦΪ���ȷ�Ӧ������HС��0���ʴ�Ϊ��3��С�ڣ�
(2)��֪��CO��H2�ı�ȼ���ȷֱ�Ϊ-283.0kJmol-1��-285.8kJmol-1����H2O(1)�TH2O(g)��H3=44.0kJmol-1����֪�Ȼ�ѧ����ʽa��CO(g)+![]() O2(g)=CO2(g)��H=-283.0kJmol-1��b��H2(g)+
O2(g)=CO2(g)��H=-283.0kJmol-1��b��H2(g)+![]() O2(g)=H2O(1)��H=-285.8kJmol-1��c��H2O(1)�TH2O(g)��H3=44.0kJmol-1���ɸ�˹���ɽ�b-a+c�ɵ�CO2(g)+H2(g)CO(g)+H2O(g)��H2 =(-285.8+283.0+44)kJmol-1=+41.2kJmol-1���ӱ������ݷ������ڴ���Cat.2�������£��״���ѡ���Ը���˵������Cat.2�Է�Ӧ����Ч�����ã������ܽ��ͷ�Ӧ�Ļ�ܣ�˵��ʹ�ô���Cat.2�ķ�Ӧ�����л�ܸ��ͣ���ͼΪ
O2(g)=H2O(1)��H=-285.8kJmol-1��c��H2O(1)�TH2O(g)��H3=44.0kJmol-1���ɸ�˹���ɽ�b-a+c�ɵ�CO2(g)+H2(g)CO(g)+H2O(g)��H2 =(-285.8+283.0+44)kJmol-1=+41.2kJmol-1���ӱ������ݷ������ڴ���Cat.2�������£��״���ѡ���Ը���˵������Cat.2�Է�Ӧ����Ч�����ã������ܽ��ͷ�Ӧ�Ļ�ܣ�˵��ʹ�ô���Cat.2�ķ�Ӧ�����л�ܸ��ͣ���ͼΪ ���ʴ�Ϊ��+41.2��
���ʴ�Ϊ��+41.2��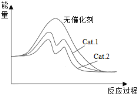 ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
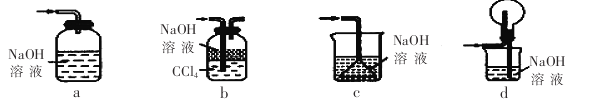
����Ŀ���������õ���ͨ���Ũ��NaOH��H2O2�Ļ��Һ�У��ڵ��ܿ�����Һ�ĽӴ�������˸�ĺ����֡�������Ϊͨ������Һ�в�����ClO����H2O2��ԭ���������ҷ�Ӧ�����������ϸߵ������ӣ�Ȼ������ת��Ϊ��ͨ�����ӣ�����������Ժ��ų�����ʵ�����õ�������������ͼ��

����Ҫ����д���пհף�
��1�� ��װ��������װ��ʱ��Ӧѡ�õ�����������Ϊ ����дͼ�б������
��2�� ��ʵ�����ʱ����������������ҵ�˳�����������ĸ����������ܵı������Ϊ ��
��3�� �����ٵ���Ƥ��������Ӧ��2����ԭ���� ��
��4�� ��ʵ��������10mol��L��1��NaOH��Һ500mL���õ�����������������ƽ���ձ��⣬�����õ���������
�������������� ������ʱ������ͼ����������ҺŨ�� ���ƫ�ߡ���ƫ�͡�����

��5�� ʵ��ʱ��������ClO����H2O2��Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200 mL��Mg2+��Al3+��NH4+��H+��Cl�� �����ӵ���Һ������μ���4 mol/L NaOH��Һ������NaOH��Һ�������mL�����������������������mol����ϵ��ͼ��ʾ������������ȷ������ ��

A��ԭ��Һ��c��H+�� = 0.08 mol/L
B��ԭ��Һ��n��Mg2+����n��Al3+�� = 10��1
C��x��y�IJ�ֵΪ0.01 mol
D��ԭ��Һ��c��Cl���� = 0.066 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ2CH3OH(g)![]() CH3OCH3(g)��H2O(g)ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶�������2 L���ܱ������м���a mol CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
CH3OCH3(g)��H2O(g)ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶�������2 L���ܱ������м���a mol CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
Ũ��/(mol��L��1) | 0.44 | 0.6 | 0.6 |
����˵����ȷ����
A������ʼʱ����2a mol CH3OH����ﵽƽ��ʱCH3OH��ת��������
B������������ƽ��Ħ���������ٱ仯����˵����Ӧ���ﵽƽ��״̬
C�� a = 1.64
D����ʱ������Ӧ���ʴ����淴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�ص�ԭ����������ij�ֳ������ϼ۵Ĺ�ϵͼ������ԭ��������������Ӧ��Ԫ�أ�������˵����ȷ����

A. 31d��33d����ͬ�ֺ���
B. ��ҵ�ϳ��õ�ⷨ�Ʊ�����b��c
C. ��̬�⻯����ȶ��ԣ�a��d��e
D. a��b�γɵĻ����ﲻ���ܺ����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����жԳ����ܽ�ƽ���������ȷ����( )
A����Ӧ��ʼʱ����Һ�и�����Ũ�����
B�������ܽ�ﵽƽ��ʱ�����������ʺ��ܽ���������
C�������ܽ�ﵽƽ��ʱ����Һ�����ʵ�����Ũ�����,�ұ��ֲ���
D�������ܽ�ﵽƽ��ʱ������ټ��������Եĸó�����,���ٽ��ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ:2NO2 ![]() 2NO+O2�ڶ����ܱ������з�Ӧ,�ﵽƽ��״̬�ı�־��( )
2NO+O2�ڶ����ܱ������з�Ӧ,�ﵽƽ��״̬�ı�־��( )
����λʱ��������n mol O2��ͬʱ����2 nmolNO2
����λʱ��������n mol O2��ͬʱ����2 nmolNO
����NO2��NO ��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ2:2:1��״̬
������������ɫ���ٸı��״̬
�����������ܶȲ��ٸı��״̬
����������ѹǿ���ٸı��״̬
����������ƽ����Է����������ٸı��״̬
��NO2 ��NO��O2�ķ�����֮��Ϊ2��2��1��״̬
A���٢ۢܢ� B�� �ڢۢݢ� C�� �٢ܢޢ� D�� �٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴Ӧ��2SO2(g)��O2(g)![]() 2SO3(g)�����д�ʩ��ʹ��Ӧ���л���Ӱٷ�������ѧ��Ӧ���ʺͻ�ѧƽ�ⳣ�����仯����
2SO3(g)�����д�ʩ��ʹ��Ӧ���л���Ӱٷ�������ѧ��Ӧ���ʺͻ�ѧƽ�ⳣ�����仯����
A������ѹǿ B�������¶� C��ʹ�ô��� D�������O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ի�ͭ������Ҫ�ɷ�CuFeS2��Ϊԭ���Ʊ�CuS04.5H2O����Ҫ�������£�

��1������װ�ò���������������X���� �������������
��2������Y�ijɷ�ΪFe203��Fe0��ѡ���ṩ���Լ������ʵ����֤�����к���FeO��
�ṩ���Լ���ϡ���ᡢϡ���ᡢKSCN��Һ��KMn04��Һ��NaOH��Һ����ˮ��
���������ṩ���Լ���ѡ��ʵ����֤����ҩƷ ��
��д����֤��������������������ԭ��Ӧ�����ӷ���ʽ ��
��3�����ͭ�м������������Ļ�����Һ��ȡ����ͭʱ�����ʲ��μӷ�Ӧ����������HNO3��H2S04��������ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com