
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础。如图为两套实验装置。

(1)写出下列实验仪器的名称A___;B___;C__;D___。
(2)用装置1分离四氯化碳和Br2的混合物,实验操作的名称为___,冷凝管的进水口是___;(填a或b);
(3)现需配制480mL 0.2mol/L KOH溶液,需要称量KOH___g,配制过程中所用到的仪器有托盘天平、烧杯、___、___、胶头滴管。
(4)装置2是某同学转移溶液的示意图,图中的错误是___。
(5)下列操作会引起浓度偏高的是___。
A.溶液未冷却到室温就转移至容量瓶中 B.称量固体时将右边放药品与左边放砝码
C.定容时仰视读数 D.容量瓶中的水未除尽
【答案】蒸馏烧瓶 酒精灯 直形冷凝管 锥形瓶 蒸馏 a 5.6 500mL容量瓶 玻璃棒 没有使用玻璃棒引流 A
【解析】
(1)A为蒸馏烧瓶,B为酒精灯,C为直形冷凝管,D为锥形瓶;
(2)该操作为蒸馏,冷静管的进水口为下口,即a;
(3)配制480mL的溶液,需要使用500mL的容量瓶去配制500mL的溶液,故需要KOH的物质的量为0.5L×0.2mol/L=0.1mol,则m(KOH)=0.1mol×56g/mol=5.6g;配制溶液需要用到的仪器有托盘天平、烧杯、500mL容量瓶、玻璃棒、胶头滴管;
(4)该操作的错误是没有使用玻璃棒引流;
(5)A、溶液未冷却到室温就转移至容量瓶中,会导致溶液体积偏小,浓度偏高,A符合题意;
B、称量固体时将右边放药品与左边放砝码,若没使用游码,则固体质量不变,溶液浓度不受影响,若使用游码,则固体质量偏小,溶液浓度偏低,B不符合题意;
C、定容时仰视,溶液体积偏大,浓度偏低,C不符合题意;
D、容量瓶中的水未除尽,但不影响定容,故对溶液浓度无影响,D不符合题意;
故选A。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)下列说法正确是( )
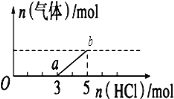
A.oa段反应的离子方程式为:H++OH-=H2O
B.O点溶液中所含溶质的化学式为NaHCO3、Na2CO3
C.标准状况下,通入CO2的体积为4.48L
D.原NaOH溶液的物质的量浓度为2.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛性能优越,被称为继铁、铝之后的“第三金属”。钛铁矿(主要成分为FeTiO3,含少量Fe2O3、SiO2等杂质)可用来制备TiO2,同时得到副产品绿矾(FeSO4·7H2O),工艺流程如图所示:
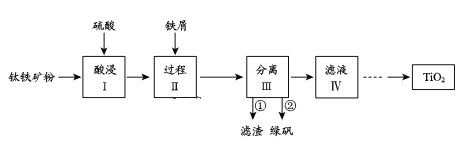
己知:①FeTiO3+2H2SO4=FeSO4+TiOSO4+2H2O
②TiO2+易水解,只能存在于强酸性溶液中
(1)酸浸I中Fe2O3与稀硫酸反应的离子方程式:_____。
(2)过程II中加入适量铁屑的目的是____。
(3)分离III中步骤②得到绿矾的操作是_____。
(4)由滤液IV提取TiO2的过程如下:
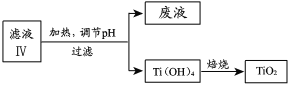
①请用化学平衡移动原理解释滤液加热煮沸的目的:______。
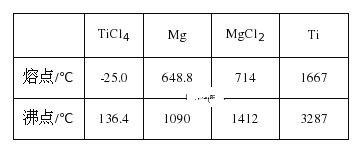
②由2Mg+TiCl4→Ti+2MgCl2反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据如表信息,需加热的温度略高于___℃即可。
③电解TiO2制备钛的方法如图所示。该方法由于具备生产过程简化、生产成本低、产品质量高、环境友好等诸多优点而引人注目。已知TiO2熔融状态下不发生电离,电解时阴极反应式为____。
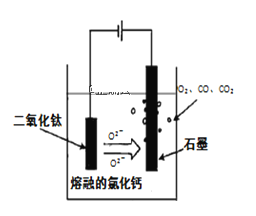
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置说法正确的是( )
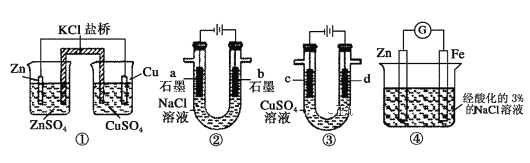
A.装置①中,一段时间后CuSO4浓度增大
B.装置②中滴入酚酞,a极附近变红
C.用装置③精炼铜时,c极为粗铜
D.装置④中发生吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法中正确的是( )
A.54g H2O中含有3NA个氢原子
B.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
C.标准状况下,NA个H2O分子所占的体积约为22.4L
D.1mol CO2和NO2的混合物中含的氧原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
3Z(g) ΔH<0,平衡时,X和Y的转化率都是10%。下列叙述不正确的是
A.m=2
B.达平衡时,Z的体积分数为10%
C.达平衡后,保持容器体积不变,加热,容器内压强将增大
D.将平衡后的容器体积压缩至1L,X的浓度为0.45mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写中正确的是
A.氢氧化镁与盐酸反应:H++OH-=H2O
B.铁与盐酸反应:2Fe+6H+=2Fe3++3H2
C.氧化铝溶于稀硫酸:Al2O3+6H+=2Fe3++3H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3 胶体:Fe3++3H2O=Fe(OH)3+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应,硼与氯气反应生成三氯化硼(BC13),生成的三氯化硼遇水水解产生白雾(已知:BC13的熔点为 -107. 3℃,沸点为12.5 ℃)。某兴趣小组设计如图所示装置制备三氯化硼。
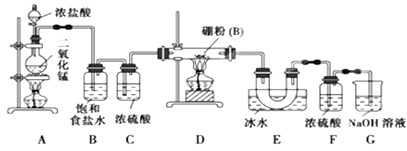
回答下列问题:
(1)写出装置A中发生反应的离子方程式________________。
(2)写出装置D中发生反应的化学方程式为_____________________。
(3)装置B、E的作用分别是________________、________________。
(4)可以用盛装____________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
(5)为了顺利完成实验,点燃酒精灯的正确操作是______(填字母),
a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯
其理由是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列化学方程式:
(1)实验室可以用KClO3和浓盐酸反应制取氯气,写出发生反应的化学方程式并用双线桥表示电子转移方向和数目_____________。
(2)二氧化氯(ClO2)作为一种高效强氧化剂,可用KClO3和草酸(H2C2O4),稀硫酸,水浴加热制备。反应后产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为________________。
(3)写出工业上制备漂白粉的化学方程式___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com