
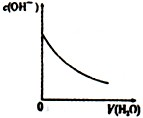
 |  |  |  |
| A.盐酸加水稀释 | B.Mg(OH)2悬浊液中滴加NH4Cl溶液 | C.NH4Cl稀溶液加水稀释 | D.NH3通入醋酸溶液中 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锂(Li)的原子失电子能力比钠弱 |
| B、砹(At)的氢化物不稳定 |
| C、H2S比水稳定 |
| D、氢氧化钠比氢氧化镁的碱性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生设计了如图的方法对X盐进行鉴定:由此分析,下列结论中不正确的是( )
某学生设计了如图的方法对X盐进行鉴定:由此分析,下列结论中不正确的是( )| A、X中可以有Fe2+ |
| B、Y为AgI沉淀 |
| C、X中可以有Fe3+ |
| D、M试剂可以是H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)2易被氧化生成Fe(OH)3,说明稳定性:Fe(OH)2<Fe(OH)3 |
| B、铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3(X=Cl、Br、I) |
| C、Fe与S加热可得FeS,所以Cu与S加热可得CuS |
| D、铁器放在潮湿的地方很容易生锈,其铁锈的主要成分Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+ |
| B、Fe2+ |
| C、Cu2+ |
| D、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流,是21世纪最富有挑战性的课题之一.最近有人设计了一种固体燃料电池,以掺杂了氧化钇的固体氧化锆为电解质.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列关于该电池的判断中,错误的是( )
设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流,是21世纪最富有挑战性的课题之一.最近有人设计了一种固体燃料电池,以掺杂了氧化钇的固体氧化锆为电解质.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列关于该电池的判断中,错误的是( )| A、该电池的正极反应式为:O2+2H2O+4e-=4OH- |
| B、氧化钇和氧化锆的化学式分别为Y2O3和ZrO2,掺杂氧化钇的氧化锆晶体中存在晶体缺陷,其导电性比纯氧化锆晶体强得多 |
| C、该燃料电池外部的电流方向为正极一负极,内部阴离子向负极移动 |
| D、燃料电池相对于汽油直接燃烧,具有较高的能量利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然果汁中不含任何化学物质 |
| B、味精的主要成分为蛋白质,烧菜时刻加入适量 |
| C、“绿色食品”是指颜色一定为绿色的食品 |
| D、烧鱼时放点醋,可软化鱼骨 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com