
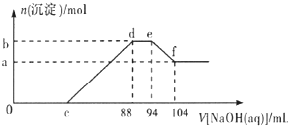
 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的 化合价越低.现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL )与产生沉淀的物质的量( mol)关系如图所示,下列说法不正确的是( )
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的 化合价越低.现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL )与产生沉淀的物质的量( mol)关系如图所示,下列说法不正确的是( )| A、稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 | B、c点对应NaOH溶液的体积为48 mL | C、b点与a点的差值为0.05 mol | D、样品中铝粉和铁粉的物质的量之比为5:3 |
| 0.2mol |
| 5mol/L |


科目:高中化学 来源: 题型:
(12分)钢铁表面发蓝(或发黑,在钢铁表面形成一层致密的氧化物Fe3O4)可提高其耐磨、耐蚀性能。其原理是:
①在NaOH溶液中,将铁粉溶解在NaNO2溶液中,除水之外,还可产生A和C。其中C为气体,能使湿润的红色石蕊试纸变蓝。
②A能在过量的NaNO2溶液中继续反应,生成B和C。
③A和B的溶液能继续反应,生成Fe3O4。
经研究发现:A和B的焰色反应均为黄色,其导电性实验均为K2SO4型。生成物中A与C、B与C的物质的量之比均为31。回答下列问题:
4-1 写出并配平化学反应方程式。
4-2 实践中发现适当提高温度或增大NaNO2溶液的浓度有利于氧化膜增厚,但加大NaOH溶液浓度对膜层厚度影响不大。试说明原因。
4-3 发蓝层遇光气(COCl2),若不及时清洗,则发蓝层的完整性将被破坏。写出有关的化学反应方程式。
4-4 有一种隐形材料D可由B与Zn(NO3)2 反应生成,也可用以硝酸铁、硝酸锌、氢氧化钠等为原料的水热合成法。请确定D的化学式,并判断上述制备D的反应是否属于氧化还原反应。此法所得产品D能够隐形的原因是什么?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com