
 Ō×ÓŠņŹżÖ®ŗĶĪŖ16µÄČżÖÖ¶ĢÖÜĘŚŌŖĖŲx”¢y”¢z¶ŌÓ¦µÄµ„ÖŹ X”¢Y”¢Z£¬³£ĪĀ³£Ń¹ĻĀ¾łĪŖĪŽÉ«ĘųĢ壬ŌŚŹŹµ±Ģõ¼žĻĀµ„ÖŹX”¢Y”¢ZÖ®¼äæÉŅŌ·¢ÉśČēĶ¼ĖłŹ¾µÄ±ä»Æ£®ŅŃÖŖB·Ö×Ó×é³ÉÖŠzŌ×ÓøöŹż±ČC·Ö×ÓÖŠÉŁŅ»øö£®
Ō×ÓŠņŹżÖ®ŗĶĪŖ16µÄČżÖÖ¶ĢÖÜĘŚŌŖĖŲx”¢y”¢z¶ŌÓ¦µÄµ„ÖŹ X”¢Y”¢Z£¬³£ĪĀ³£Ń¹ĻĀ¾łĪŖĪŽÉ«ĘųĢ壬ŌŚŹŹµ±Ģõ¼žĻĀµ„ÖŹX”¢Y”¢ZÖ®¼äæÉŅŌ·¢ÉśČēĶ¼ĖłŹ¾µÄ±ä»Æ£®ŅŃÖŖB·Ö×Ó×é³ÉÖŠzŌ×ÓøöŹż±ČC·Ö×ÓÖŠÉŁŅ»øö£® £®
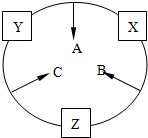
£® ·ÖĪö Ō×ÓŠņŹżÖ®ŗĶĪŖ16µÄČżÖÖ¶ĢÖÜĘŚŌŖĖŲµÄµ„ÖŹX”¢Y”¢Z£¬³£ĪĀ³£Ń¹ĻĀ¾łĪŖĪŽÉ«ĘųĢ壬ŌņÕāČżÖÖĘųĢåŹĒµŖĘų”¢ŃõĘųŗĶĒāĘų£ØĻ”ÓŠĘųĢå³żĶā£©£¬Éś³ÉµÄČżÖÖ»ÆŗĻĪļÓŠNO”¢H2O”¢NH3£¬B·Ö×Ó×é³ÉÖŠzŌ×ÓøöŹż±ČC·Ö×ÓÖŠÉŁŅ»øö£¬±Č½ĻÕāČżÖÖ·Ö×ÓÖŖ£¬Ö»ÓŠĖ®·Ö×ÓÖŠµÄHŌ×ӱȰ±Ęų·Ö×ÓÖŠµÄĒāŌ×ÓÉŁŅ»øö£¬ĖłŅŌZĪŖHŌŖĖŲ£¬A·Ö×ÓĪŖNO£¬B·Ö×ÓĪŖH2O£¬C·Ö×ÓĪŖNH3£¬ĖłŅŌYŹĒNŌŖĖŲ£¬XĪŖOŌŖĖŲ£¬½įŗĻĪļÖŹµÄ½į¹¹ŠŌÖŹ½ā“š£®
½ā“š ½ā£ŗŌ×ÓŠņŹżÖ®ŗĶĪŖ16µÄČżÖÖ¶ĢÖÜĘŚŌŖĖŲµÄµ„ÖŹX”¢Y”¢Z£¬³£ĪĀ³£Ń¹ĻĀ¾łĪŖĪŽÉ«ĘųĢ壬ŌņÕāČżÖÖĘųĢåŹĒµŖĘų”¢ŃõĘųŗĶĒāĘų£ØĻ”ÓŠĘųĢå³żĶā£©£¬Éś³ÉµÄČżÖÖ»ÆŗĻĪļÓŠNO”¢H2O”¢NH3£¬B·Ö×Ó×é³ÉÖŠzŌ×ÓøöŹż±ČC·Ö×ÓÖŠÉŁŅ»øö£¬±Č½ĻÕāČżÖÖ·Ö×ÓÖŖ£¬Ö»ÓŠĖ®·Ö×ÓÖŠµÄHŌ×ӱȰ±Ęų·Ö×ÓÖŠµÄĒāŌ×ÓÉŁŅ»øö£¬ĖłŅŌZĪŖHŌŖĖŲ£¬A·Ö×ÓĪŖNO£¬B·Ö×ÓĪŖH2O£¬C·Ö×ÓĪŖNH3£¬ĖłŅŌYŹĒNŌŖĖŲ£¬XĪŖOŌŖĖŲ£¬
£Ø1£©YŹĒNŌŖĖŲ£¬¶ŌÓ¦µÄµ„ÖŹĪŖµŖĘų£¬½į¹¹Ź½ĪŖN”ŌN£¬¹Ź“š°øĪŖ£ŗN”ŌN£»
£Ø2£©XĪŖŃõĘų£¬CĪŖ°±Ęų£¬ŌŚ“߻ƼĮ”¢¼ÓČČĢõ¼žĻĀ£¬°±ĘųŗĶŃõĘų·“Ӧɜ³ÉŅ»Ńõ»ÆµŖŗĶĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£¬
¹Ź“š°øĪŖ£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£»
£Ø3 £©³£ĪĀĻĀ£¬C£ØNH3£©µÄĖ®ČÜŅŗÄܹ»Ź¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£¬±äĄ¶µÄŌŅņŹĒ£ŗNH3•H2O?NH4++OH-£¬¹Ź“š°øĪŖ£ŗNH3•H2O?NH4++OH-£»
£Ø4£©NOŗĶ°±Ęų·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĖ®ŗĶµŖĘų£¬·½³ĢŹ½ĪŖ6NO+4NH3ØT5N2+6H2O£¬¹Ź“š°øĪŖ£ŗ6NO+4NH3ØT5N2+6H2O£»
£Ø5£©Į½øöĒāŌ×ÓŗĶŃõŌ×Ó¹²ÓƵē×Ó¶Ō¶ųŠĪ³É¹²¼Ū¼ü£¬ĘäŠĪ³É¹ż³ĢĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌŖĖŲ»ÆŗĻĪļÖŹµÄĶʶĻ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬±¾ĢāŅŌ”°B·Ö×Ó×é³ÉÖŠZŌ×ÓøöŹż±ČC·Ö×ÓÖŠÉŁŅ»øö”±ĪŖĢāŃŪ½ųŠŠĶʶĻ£¬½įŗĻĪļÖŹµÄ»ÆѧŹ½Ą“·ÖĪö½ā“š£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 9£ŗ1£ŗ6 | B£® | 3£ŗ1£ŗ2 | C£® | 3£ŗ2£ŗ2 | D£® | 9£ŗ2£ŗ6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 50ml0.50mol•L-1ŃĪĖįÓė50mL0.55mol•L-1NaOHČÜŅŗŌŚČēĻĀĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠ·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
50ml0.50mol•L-1ŃĪĖįÓė50mL0.55mol•L-1NaOHČÜŅŗŌŚČēĻĀĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ½ųŠŠÖŠŗĶ·“Ó¦£®Ķعż²ā¶Ø·“Ó¦¹ż³ĢÖŠ·Å³öµÄČČĮææɼĘĖćÖŠŗĶČČ£®»Ų“šĻĀĮŠĪŹĢā£ŗ| ŹµŃéŠņŗÅ | ĘšŹ¼ĪĀ¶Čt1/”ę | ÖÕÖ¹ĪĀ¶Č£Øt2£©”ę | ĪĀ²ī£Øt2-t1£©”ę | ||
| ŃĪĖį | NaOHČÜŅŗ | Ę½¾łÖµ | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.0 | 3.0 |
| 2 | 25.1 | 25.1 | 25.1 | 28.2 | 3.1 |
| 3 | 25.1 | 25.1 | 25.1 | 28.3 | 3.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·śĄū°ŗ£ØCCl2F2£©ŅņĘĘ»µ“óĘų³ōŃõ²ć¶ųµ¼ÖĀ”°ĪĀŹŅŠ§Ó¦”± | |
| B£® | ½«Ą¬»ų·ÖĄą²¢»ŲŹÕĄūÓĆŹĒĄ¬»ų“¦ĄķµÄ·¢Õ¹·½Ļņ | |
| C£® | ·Ļ¾Éµē³ŲµÄ»ŲŹÕ£¬ĘäÖ÷ŅŖÄæµÄŹĒ±£»¤»·¾³£¬¶ų²»ŹĒ»ŲŹÕ½šŹō | |
| D£® | µķ·Ū²Ķ¾ß±»ČĻĪŖŹĒÓŠ·¢Õ¹Ē°¾°µÄŅ»“ĪŠŌ²Ķ¾ß£¬æÉÓŠĄūÓŚ±£»¤»·¾³ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
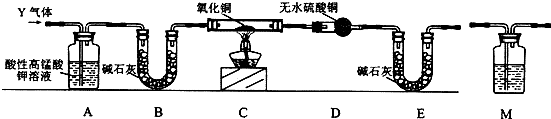
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1molČĪŗĪĘųĢåµÄĢå»ż¶¼ŹĒ22.4L | |
| B£® | 1mol H2µÄÖŹĮæŹĒ1g£¬ĖüĖłÕ¼µÄĢå»żŹĒ22.4L | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬1molČĪŗĪĘųĢåĖłÕ¼µÄĢå»ż¶¼Ō¼ĪŖ22.4L•mol-1 | |
| D£® | ŌŚ±ź×¼×“æöĻĀ£¬1molČĪŗĪĘųĢåĖłÕ¼µÄĢå»ż¶¼Ō¼ĪŖ22.4L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| ŌŖĖŲ±ąŗÅ | ŌŖĖŲŠŌÖŹ»ņŌ×Ó½į¹¹ |
| T | µ„ÖŹŹĒŅ»ÖÖµ»ĘÉ«¹ĢĢ壬ŹĒŗŚ»šŅ©³É·ÖÖ®Ņ» |
| X | ×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶ |
| Y | ³£ĪĀĻĀµ„ÖŹĪŖĖ«Ō×Ó·Ö×Ó£¬ĘäĒā»ÆĪļĖ®ČÜŅŗ³Ź¼īŠŌ |
| Z | ŌŖĖŲ×īøßÕż¼ŪŹĒ+7¼Ū |
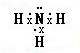 £¬ĘäĖ®ČÜŅŗ³Ź¼īŠŌµÄŌŅņŹĒ£ØÓƵēĄė·½³ĢŹ½±ķŹ¾£©£ŗNH3•H2O?NH4++OH-£®
£¬ĘäĖ®ČÜŅŗ³Ź¼īŠŌµÄŌŅņŹĒ£ØÓƵēĄė·½³ĢŹ½±ķŹ¾£©£ŗNH3•H2O?NH4++OH-£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2æÉŅŌÓĆĄ“ĘÆ°×Ö½½¬”¢Ć«”¢Ė攢²ŻĆ±±č”¢Ōö°×Ź³Ę·µČ | |
| B£® | Ķ؊ŹāĄĀµÄÖ÷ŅŖ³É·ÖŹĒ¾§ĢåSi£¬Ģ«ŃōÄܵē³ŲµÄ²ÄĮĻÖ÷ŅŖŹĒSiO2 | |
| C£® | øßĆĢĖį¼ŲČÜŅŗ”¢¾Ę¾«”¢Ė«ŃõĖ®¶¼ÄÜɱ¾śĻū¶¾£¬¶¼ĄūÓĆĮĖĒæŃõ»ÆŠŌ | |
| D£® | °±ŗÜČŻŅ×Ņŗ»Æ£¬Ņŗ°±Ęų»ÆĪüŹÕ“óĮæµÄČČ£¬ĖłŅŌŅŗ°±³£ÓĆ×÷ÖĀĄä¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
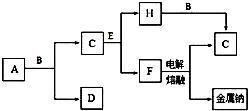 ֊ѧ»Æѧ֊³£¼ūµÄ¼øÖÖĪļÖŹ“ęŌŚČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£¬ĘäÖŠ£¬AŹĒŅ»ÖÖŗŚÉ«·Ūĩד¹ĢĢ壬CŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壮ŹµŃéŹŅÖŠ³£ÓĆEČÜŅŗĪüŹÕ¶ąÓąµÄC£®£ØĶ¼ÖŠ²æ·Ö²śĪļŗĶ·“Ó¦Ģõ¼žŅŃĀŌČ„£©£®
֊ѧ»Æѧ֊³£¼ūµÄ¼øÖÖĪļÖŹ“ęŌŚČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£¬ĘäÖŠ£¬AŹĒŅ»ÖÖŗŚÉ«·Ūĩד¹ĢĢ壬CŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壮ŹµŃéŹŅÖŠ³£ÓĆEČÜŅŗĪüŹÕ¶ąÓąµÄC£®£ØĶ¼ÖŠ²æ·Ö²śĪļŗĶ·“Ó¦Ģõ¼žŅŃĀŌČ„£©£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com